薬効分類名禁煙補助薬
一般的名称ニコチン
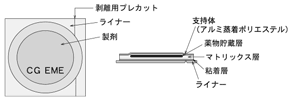
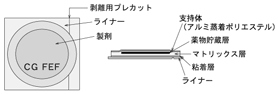
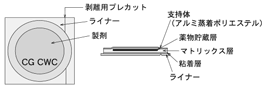
ニコチネルTTS30、ニコチネルTTS20、ニコチネルTTS10
Nicotinell TTS 30, Nicotinell TTS 20, Nicotinell TTS 10
製造販売元(輸入)/Haleonジャパン株式会社、販売元/アルフレッサファーマ株式会社
重大な副作用
その他の副作用
併用注意
アドレナリン遮断薬
本剤との併用により、アドレナリン遮断性の薬剤の作用を減弱させるおそれがある。必要に応じてアドレナリン遮断性の薬剤を増量するなど用量に注意すること。
ニコチンにより血中コルチゾール、カテコラミンの量が増加する。
アドレナリン作動薬
本剤との併用により、アドレナリン作動性の薬剤の作用を増強させるおそれがある。必要に応じてアドレナリン作動性の薬剤を減量するなど用量に注意すること。
ニコチンにより血中コルチゾール、カテコラミンの量が増加する。
4. 効能又は効果
循環器疾患、呼吸器疾患、消化器疾患、代謝性疾患等の基礎疾患を持ち、医師により禁煙が必要と診断された禁煙意志の強い喫煙者が、医師の指導の下に行う禁煙の補助
5. 効能又は効果に関連する注意
- 5.1 本剤は禁煙意志が強く、循環器疾患、呼吸器疾患、消化器疾患、代謝性疾患等の基礎疾患を持つ患者であって、禁煙の困難な喫煙者に使用すること。
- 5.2 心疾患患者に本剤を使用する場合、問診、心電図、血圧測定、運動負荷試験等により症状が安定であることを確認すること。
- 5.3 本剤の使用は禁煙意志の強い喫煙者の禁煙補助を目的としている。このことを患者に十分説明し、禁煙宣誓書等により禁煙意志の強いことを確認してから使用すること。
- 5.4 禁煙の成功は、禁煙指導の質及び頻度に依存するので、本剤は、医師等による適切な禁煙指導の下に禁煙計画・指導の補助として用いること。また、本剤使用後も禁煙を維持させるため、禁煙指導を実施すること。
6. 用法及び用量
ニコチネルTTS10(ニコチンとして17.5mg含有)、ニコチネルTTS20(ニコチンとして35mg含有)又はニコチネルTTS30(ニコチンとして52.5mg含有)を1日1回1枚、24時間貼付する。通常、最初の4週間はニコチネルTTS30から貼付し、次の2週間はニコチネルTTS20を貼付し、最後の2週間はニコチネルTTS10を貼付する。なお、最初の4週間に減量の必要が生じた場合は、ニコチネルTTS20を貼付する。
本剤は10週間を超えて継続投与しないこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 心筋梗塞、狭心症(異型狭心症等)の既往歴のある患者、又は狭心症で症状の安定している患者
症状が再発又は悪化するおそれがある。
-
9.1.2 高血圧、不整脈、脳血管障害、心不全、末梢血管障害(バージャー病等)のある患者
症状が悪化するおそれがある。
-
9.1.3 甲状腺機能亢進症、褐色細胞腫又はパラガングリオーマ等の内分泌疾患のある患者
症状が悪化するおそれがある。
-
9.1.4 糖尿病(インスリンを使用している)患者
症状が悪化するおそれがある。また、本剤の使用にかかわらず、禁煙によりインスリンの皮下吸収が増加することが知られているので、インスリンの用量調節が必要となる場合がある。
-
9.1.5 消化性潰瘍のある患者
症状が悪化するおそれがある。
-
9.1.6 アトピー性皮膚炎あるいは湿疹性皮膚炎等の全身性皮膚疾患の患者
症状が悪化するおそれがある。
-
9.1.7 てんかん又はその既往歴のある患者
痙攣を引き起こすおそれがある。
-
9.1.8 神経筋接合部疾患(重症筋無力症、イートン・ランバート症候群)又はその既往歴のある患者
筋力低下等の症状が悪化するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には使用しないこと。ニコチンでは、動物実験で、マウスにおいて、催奇形作用(四肢の骨格異常)、胎児死亡増加、胎児体重減少、ラットにおいて、胎児死亡増加、胚の発育遅延、着床遅延、分娩開始遅延、出生児発育遅延、出生児の行動異常等が報告されている。
9.6 授乳婦
使用しないこと。ヒト母乳中へ移行することが報告されている。
9.8 高齢者
一般に生理機能が低下しているので、注意すること。
10. 相互作用
- 喫煙により肝代謝酵素CYP1A2が活性化されることが知られている。
喫煙中に下記薬剤を服用している場合、本剤を使用して禁煙を開始後、下記薬剤の作用が増強するおそれがある。
フェナセチン、カフェイン、テオフィリン、イミプラミン、ペンタゾシン、フロセミド、プロプラノロール、ロピニロール、クロザピン、オランザピン
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
アドレナリン遮断薬 |
本剤との併用により、アドレナリン遮断性の薬剤の作用を減弱させるおそれがある。必要に応じてアドレナリン遮断性の薬剤を増量するなど用量に注意すること。 |
ニコチンにより血中コルチゾール、カテコラミンの量が増加する。 |
アドレナリン作動薬 |
本剤との併用により、アドレナリン作動性の薬剤の作用を増強させるおそれがある。必要に応じてアドレナリン作動性の薬剤を減量するなど用量に注意すること。 |
ニコチンにより血中コルチゾール、カテコラミンの量が増加する。 |
11. 副作用
11.2 その他の副作用
頻度不明 |
5%以上 |
0.1~5%未満 |
0.1%未満 |
|
|---|---|---|---|---|
皮膚 |
― |
一次刺激性の接触皮膚炎(紅斑、そう痒) |
一次刺激性の接触皮膚炎(丘疹、腫脹、小水疱、刺激感)、皮膚剥離、色素沈着 |
一次刺激性の接触皮膚炎(熱感等) |
精神神経系 |
神経過敏、錯感覚、振戦、不安、抑うつ気分 |
不眠 |
頭痛、めまい、けん怠感、異夢、悪夢、集中困難 |
疲労、しびれ、眠気、易刺激性、感情不安定 |
消化器 |
― |
― |
嘔気、嘔吐、腹痛、口内炎、下痢、食欲不振 |
胸やけ、便秘、消化不良 |
肝臓 |
― |
― |
ALT(GPT)、LDH、γ-GTP、総ビリルビン値の上昇 |
AST(GOT)上昇 |
循環器 |
― |
― |
血圧上昇、動悸 |
不整脈 |
自律神経系 |
― |
― |
口渇、ほてり、多汗 |
顔面蒼白、唾液過多 |
感覚器系 |
霧視 |
― |
味覚倒錯(口中苦味感、味覚異常) |
耳鳴 |
呼吸器系 |
咳嗽 |
― |
― |
息苦しさ、咽頭違和感 |
筋・骨格系 |
背部痛 |
― |
― |
筋肉痛、肩こり、関節痛 |
過敏症 |
― |
― |
そう痒、発疹、アレルギー性接触皮膚炎、全身性蕁麻疹 |
粃糠疹(ふけの増加) |
その他 |
― |
― |
疼痛、ニコチン臭、トリグリセリド上昇、不快感 |
胸痛、浮腫、寒気、無力症、貼付上肢の重感 |
4. 効能又は効果
循環器疾患、呼吸器疾患、消化器疾患、代謝性疾患等の基礎疾患を持ち、医師により禁煙が必要と診断された禁煙意志の強い喫煙者が、医師の指導の下に行う禁煙の補助
5. 効能又は効果に関連する注意
- 5.1 本剤は禁煙意志が強く、循環器疾患、呼吸器疾患、消化器疾患、代謝性疾患等の基礎疾患を持つ患者であって、禁煙の困難な喫煙者に使用すること。
- 5.2 心疾患患者に本剤を使用する場合、問診、心電図、血圧測定、運動負荷試験等により症状が安定であることを確認すること。
- 5.3 本剤の使用は禁煙意志の強い喫煙者の禁煙補助を目的としている。このことを患者に十分説明し、禁煙宣誓書等により禁煙意志の強いことを確認してから使用すること。
- 5.4 禁煙の成功は、禁煙指導の質及び頻度に依存するので、本剤は、医師等による適切な禁煙指導の下に禁煙計画・指導の補助として用いること。また、本剤使用後も禁煙を維持させるため、禁煙指導を実施すること。
6. 用法及び用量
ニコチネルTTS10(ニコチンとして17.5mg含有)、ニコチネルTTS20(ニコチンとして35mg含有)又はニコチネルTTS30(ニコチンとして52.5mg含有)を1日1回1枚、24時間貼付する。通常、最初の4週間はニコチネルTTS30から貼付し、次の2週間はニコチネルTTS20を貼付し、最後の2週間はニコチネルTTS10を貼付する。なお、最初の4週間に減量の必要が生じた場合は、ニコチネルTTS20を貼付する。
本剤は10週間を超えて継続投与しないこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 心筋梗塞、狭心症(異型狭心症等)の既往歴のある患者、又は狭心症で症状の安定している患者
症状が再発又は悪化するおそれがある。
-
9.1.2 高血圧、不整脈、脳血管障害、心不全、末梢血管障害(バージャー病等)のある患者
症状が悪化するおそれがある。
-
9.1.3 甲状腺機能亢進症、褐色細胞腫又はパラガングリオーマ等の内分泌疾患のある患者
症状が悪化するおそれがある。
-
9.1.4 糖尿病(インスリンを使用している)患者
症状が悪化するおそれがある。また、本剤の使用にかかわらず、禁煙によりインスリンの皮下吸収が増加することが知られているので、インスリンの用量調節が必要となる場合がある。
-
9.1.5 消化性潰瘍のある患者
症状が悪化するおそれがある。
-
9.1.6 アトピー性皮膚炎あるいは湿疹性皮膚炎等の全身性皮膚疾患の患者
症状が悪化するおそれがある。
-
9.1.7 てんかん又はその既往歴のある患者
痙攣を引き起こすおそれがある。
-
9.1.8 神経筋接合部疾患(重症筋無力症、イートン・ランバート症候群)又はその既往歴のある患者
筋力低下等の症状が悪化するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には使用しないこと。ニコチンでは、動物実験で、マウスにおいて、催奇形作用(四肢の骨格異常)、胎児死亡増加、胎児体重減少、ラットにおいて、胎児死亡増加、胚の発育遅延、着床遅延、分娩開始遅延、出生児発育遅延、出生児の行動異常等が報告されている。
9.6 授乳婦
使用しないこと。ヒト母乳中へ移行することが報告されている。
9.8 高齢者
一般に生理機能が低下しているので、注意すること。
10. 相互作用
- 喫煙により肝代謝酵素CYP1A2が活性化されることが知られている。
喫煙中に下記薬剤を服用している場合、本剤を使用して禁煙を開始後、下記薬剤の作用が増強するおそれがある。
フェナセチン、カフェイン、テオフィリン、イミプラミン、ペンタゾシン、フロセミド、プロプラノロール、ロピニロール、クロザピン、オランザピン
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
アドレナリン遮断薬 |
本剤との併用により、アドレナリン遮断性の薬剤の作用を減弱させるおそれがある。必要に応じてアドレナリン遮断性の薬剤を増量するなど用量に注意すること。 |
ニコチンにより血中コルチゾール、カテコラミンの量が増加する。 |
アドレナリン作動薬 |
本剤との併用により、アドレナリン作動性の薬剤の作用を増強させるおそれがある。必要に応じてアドレナリン作動性の薬剤を減量するなど用量に注意すること。 |
ニコチンにより血中コルチゾール、カテコラミンの量が増加する。 |
11. 副作用
11.2 その他の副作用
頻度不明 |
5%以上 |
0.1~5%未満 |
0.1%未満 |
|
|---|---|---|---|---|
皮膚 |
― |
一次刺激性の接触皮膚炎(紅斑、そう痒) |
一次刺激性の接触皮膚炎(丘疹、腫脹、小水疱、刺激感)、皮膚剥離、色素沈着 |
一次刺激性の接触皮膚炎(熱感等) |
精神神経系 |
神経過敏、錯感覚、振戦、不安、抑うつ気分 |
不眠 |
頭痛、めまい、けん怠感、異夢、悪夢、集中困難 |
疲労、しびれ、眠気、易刺激性、感情不安定 |
消化器 |
― |
― |
嘔気、嘔吐、腹痛、口内炎、下痢、食欲不振 |
胸やけ、便秘、消化不良 |
肝臓 |
― |
― |
ALT(GPT)、LDH、γ-GTP、総ビリルビン値の上昇 |
AST(GOT)上昇 |
循環器 |
― |
― |
血圧上昇、動悸 |
不整脈 |
自律神経系 |
― |
― |
口渇、ほてり、多汗 |
顔面蒼白、唾液過多 |
感覚器系 |
霧視 |
― |
味覚倒錯(口中苦味感、味覚異常) |
耳鳴 |
呼吸器系 |
咳嗽 |
― |
― |
息苦しさ、咽頭違和感 |
筋・骨格系 |
背部痛 |
― |
― |
筋肉痛、肩こり、関節痛 |
過敏症 |
― |
― |
そう痒、発疹、アレルギー性接触皮膚炎、全身性蕁麻疹 |
粃糠疹(ふけの増加) |
その他 |
― |
― |
疼痛、ニコチン臭、トリグリセリド上昇、不快感 |
胸痛、浮腫、寒気、無力症、貼付上肢の重感 |