薬効分類名カルバペネム系抗生物質製剤
一般的名称メロペネム水和物
メロペネム点滴静注用0.25g「日医工」、メロペネム点滴静注用0.5g「日医工」
めろぺねむてんてきじょうちゅうよう0.25g「にちいこう」、めろぺねむてんてきじょうちゅうよう0.5g「にちいこう」
Meropenem for I.V. Infusion, Meropenem for I.V. Infusion
製造販売元/日医工ファーマ株式会社、販売元/日医工株式会社
重大な副作用
その他の副作用
2. 禁忌(次の患者には投与しないこと)
- 2.1 本剤の成分に対し過敏症の既往歴のある患者[9.1.1 参照]
- 2.2 バルプロ酸ナトリウム投与中の患者[10.1 参照]
4. 効能又は効果
-
一般感染症
-
〈適応菌種〉
メロペネムに感性のブドウ球菌属、レンサ球菌属、肺炎球菌、腸球菌属、髄膜炎菌、モラクセラ(ブランハメラ)・カタラーリス、大腸菌、シトロバクター属、クレブシエラ属、エンテロバクター属、セラチア属、プロテウス属、プロビデンシア属、インフルエンザ菌、シュードモナス属、緑膿菌、バークホルデリア・セパシア、バクテロイデス属、プレボテラ属
-
〈適応症〉
敗血症、深在性皮膚感染症、リンパ管・リンパ節炎、外傷・熱傷及び手術創等の二次感染、肛門周囲膿瘍、骨髄炎、関節炎、扁桃炎(扁桃周囲膿瘍を含む)、肺炎、肺膿瘍、膿胸、慢性呼吸器病変の二次感染、複雑性膀胱炎、腎盂腎炎、腹膜炎、胆嚢炎、胆管炎、肝膿瘍、子宮内感染、子宮付属器炎、子宮旁結合織炎、化膿性髄膜炎、眼内炎(全眼球炎を含む)、中耳炎、副鼻腔炎、顎骨周辺の蜂巣炎、顎炎
-
〈適応菌種〉
- 発熱性好中球減少症
5. 効能又は効果に関連する注意
-
〈効能共通〉
- 5.1 本剤投与前に感受性の確認が行えなかった場合、本剤投与開始後3日を目安として本剤に対する感受性を確認し、本剤投与が適正であるか判断すること。なお、本剤に感受性が認められない場合、速やかに他の薬剤に変更すること。[8.3 参照]
-
〈扁桃炎(扁桃周囲膿瘍を含む)、中耳炎、副鼻腔炎〉
- 5.2 「抗微生物薬適正使用の手引き」1) を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
-
〈発熱性好中球減少症〉
- 5.3 本剤は、以下の2条件を満たす症例に投与すること。
- 5.4 国内外のガイドライン等を参照し、本疾患の治療に十分な経験を持つ医師のもとで、本剤の使用が適切と判断される症例についてのみ実施すること。
- 5.5 本剤投与前に血液培養等の検査を実施すること。起炎菌が判明した際には、本剤投与継続の必要性を検討すること。
- 5.6 本剤投与の開始時期の指標である好中球数が緊急時等で確認できない場合には、白血球数の半数を好中球数として推定すること。
- 5.7 好中球数、発熱の回復が認められた場合には、本剤の投与中止を考慮すること。
- 5.8 腫瘍熱・薬剤熱等の非感染性の発熱であることが確認された場合には、速やかに本剤の投与を中止すること。
6. 用法及び用量
-
〈効能共通〉
本剤の使用に際しては、投与開始後3日を目安としてさらに継続投与が必要か判定し、投与中止又はより適切な他剤に切り替えるべきか検討を行うこと。
- 〈一般感染症〉
-
化膿性髄膜炎以外の一般感染症
通常、成人にはメロペネムとして、1日0.5~1g(力価)を2~3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜増減するが、重症・難治性感染症には、1回1g(力価)を上限として、1日3g(力価)まで増量することができる。
通常、小児にはメロペネムとして、1日30~60mg(力価)/kgを3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜増減するが、重症・難治性感染症には、1日120mg(力価)/kgまで増量することができる。ただし、成人における1日最大用量3g(力価)を超えないこととする。 -
化膿性髄膜炎
通常、成人にはメロペネムとして、1日6g(力価)を3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜減量する。
通常、小児にはメロペネムとして、1日120mg(力価)/kgを3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜減量する。ただし、成人における1日用量6g(力価)を超えないこととする。 -
〈発熱性好中球減少症〉
通常、成人にはメロペネムとして、1日3g(力価)を3回に分割し、30分以上かけて点滴静注する。
通常、小児にはメロペネムとして、1日120mg(力価)/kgを3回に分割し、30分以上かけて点滴静注する。ただし、成人における1日用量3g(力価)を超えないこととする。
7. 用法及び用量に関連する注意
-
7.1 腎機能障害のある患者では、次表を目安に本剤の投与量及び投与間隔を調節するなど、患者の状態を観察しながら慎重に投与すること。[9.2 参照],[16.6.1 参照]
Ccr※が50mL/min以下の腎機能障害患者(成人)の投与量、投与間隔の目安 Ccr(mL/min)
投与量、投与間隔
26~50
1回あたりの投与量を減量せず
12時間ごとに投与10~25
1回あたりの投与量を1/2に減量し
12時間ごとに投与<10
1回あたりの投与量を1/2に減量し
24時間ごとに投与※クレアチニンクリアランス
- 7.2 血液透析日には、透析終了後に投与すること。[13.1 参照]
8. 重要な基本的注意
-
8.1 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.1 参照]
- 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。[9.1.1 参照]
- 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
- 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
- 8.2 投与後3~5日目までは発疹等の副作用の発現には特に注意し、症状が発現したときには、他剤に切り替えるなど適切な処置を講じること。なお、継続使用にあたっても、引き続き副作用症状に注意すること。[11.1.7 参照]
- 8.3 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。[5.1 参照]
- 8.4 患者の状態から判断して、やむを得ず原因菌不明のまま本剤を使用した場合、数日間以内に改善の徴候が認められないときには、他剤に切り替えるなど適切な処置を講じること。なお、継続使用にあたっても、引き続き症状の改善等から判断し、漫然と長期の投与を行わないこと。
- 8.5 患者の状態等から判断して、7日以上にわたって本剤を投与する場合には、その理由を常時明確にし、発疹の出現や肝機能異常等の副作用に留意し、漫然とした継続投与は行わないこと。
- 8.6 AST、ALTの上昇があらわれることがあるので、1週間以上の使用に際しては、必ず肝機能検査を実施すること。
- 8.7 急性腎障害等の重篤な腎機能障害、劇症肝炎、肝機能障害、黄疸、汎血球減少、無顆粒球症、溶血性貧血、白血球減少、血小板減少があらわれることがあるので、定期的に臨床検査(腎機能検査、肝機能検査、血液検査等)を行うこと。[11.1.2 参照],[11.1.3 参照],[11.1.8 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
- 9.1.1 カルバペネム系、ペニシリン系又はセフェム系抗生物質に対し過敏症の既往歴のある患者(ただし、本剤に対し過敏症の既往歴のある患者には投与しないこと)
- 9.1.2 本人又は両親、兄弟に気管支喘息、発疹、じん麻疹等のアレルギー症状を起こしやすい体質を有する患者
-
9.1.3 経口摂取の不良な患者又は非経口栄養の患者、全身状態の悪い患者
ビタミンK欠乏症状があらわれることがある。
-
9.1.4 てんかんの既往歴あるいは中枢神経障害を有する患者
痙攣、意識障害等の中枢神経症状が起こりやすい。[11.1.6 参照]
9.2 腎機能障害患者
痙攣、意識障害等の中枢神経症状が起こりやすい。[7.1 参照],[11.1.6 参照],[16.6.1 参照]
9.3 肝機能障害患者
-
9.3.1 高度の肝機能障害のある患者
肝機能障害が悪化するおそれがある。[11.1.3 参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒト母乳中へ移行することが報告されている2) 。
9.7 小児等
低出生体重児、新生児を対象とした臨床試験は実施していない。国内の小児臨床試験では、軽度のAST、ALT上昇が多く報告されている。
11. 副作用
11.1 重大な副作用
-
11.1.1 ショック、アナフィラキシー(いずれも0.1%未満)
呼吸困難、不快感、口内異常感、喘鳴、眩暈、便意、耳鳴、発汗、全身潮紅、血管浮腫、じん麻疹等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。[8.1 参照]
- 11.1.2 急性腎障害等の重篤な腎機能障害(0.1%未満)
- 11.1.3 劇症肝炎(頻度不明)、肝機能障害(0.1~5%未満)、黄疸(0.1%未満)
-
11.1.4 偽膜性大腸炎等の血便を伴う重篤な大腸炎(0.1%未満)
腹痛、頻回の下痢があらわれた場合には直ちに投与を中止するなど適切な処置を行うこと。
-
11.1.5 間質性肺炎、PIE症候群(いずれも0.1%未満)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多等があらわれた場合には投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
- 11.1.6 痙攣、意識障害等の中枢神経症状(0.1%未満)
- 11.1.7 **中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(0.1%未満)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、急性汎発性発疹性膿疱症(頻度不明)
- 11.1.8 汎血球減少、無顆粒球症、溶血性貧血(いずれも頻度不明)、白血球減少、血小板減少(いずれも0.1%未満)
- 11.1.9 血栓性静脈炎(頻度不明)
11.2 その他の副作用
0.1~5%未満 |
0.1%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹、発熱 |
じん麻疹、紅斑、そう痒、発赤 |
熱感 |
血液 |
顆粒球減少、好酸球増多、血小板減少又は増多、赤血球減少、ヘモグロビンの減少 |
好塩基球増多、リンパ球増多、好中球増多、単球増多、ヘマトクリットの減少、異型リンパ球出現 |
|
肝臓 |
AST、ALT、LDH、ALP、LAP、γ-GTP、ビリルビン、尿ウロビリノーゲンの上昇 |
黄疸、コリンエステラーゼ低下 |
|
腎臓 |
BUN、クレアチニンの上昇 |
尿中β2-マイクログロブリンの上昇、尿蛋白陽性 |
|
消化器 |
下痢 |
嘔気、嘔吐、腹痛 |
食欲不振 |
菌交代症 |
口内炎、カンジダ症 |
||
ビタミン欠乏症 |
ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
||
その他 |
血清カリウム上昇 |
頭痛、倦怠感、不穏、血清ナトリウム低下、血清カリウム低下、CK上昇、トリグリセリド増加、胸部不快感、血中尿酸減少又は増加、注射部位反応(炎症、疼痛、硬結等) |
ミオクローヌス、せん妄 |
13. 過量投与
-
13.1 処置
本剤は血液透析又は血液ろ過により除去される。[7.2 参照]
14. 適用上の注意
14.1 薬剤調製時の注意
- 14.1.1 本剤溶解時、溶液は無色から微黄色澄明を呈するが、色の濃淡は本剤の効力には影響しない。
- 14.1.2 溶解後は速やかに使用すること。なお、やむを得ず保存を必要とする場合でも、日局生理食塩液に溶解した場合、室温保存では6時間以内に、5℃保存では24時間以内に使用すること。[14.1.4 参照]
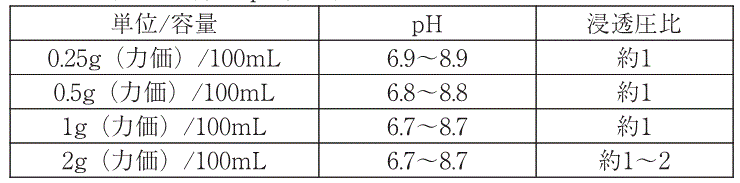
- 14.1.3 通常0.25g~2.0g(力価)当たり100mL以上の日局生理食塩液等に溶解する。ただし、注射用水は等張にならないので使用しないこと。
-
14.1.4 主な輸液との配合変化
0.5gバイアル製剤を、25±2℃で主な輸液に溶解したとき、本剤の残存力価が90%以上を示した時間は下表のとおりである。[14.1.2 参照]
輸 液
残存力価90%以上を示した時間
(hr)名 称
容量
(mL)生理食塩液
10
1006
245%ブドウ糖注射液
10
1003
6キリット注5%
500
6
果糖注射液5%
500
6
アクチット輸液
200
6
10%EL-3号輸液
500
6
KN3号輸液
200
5003
6ソリタ-T3号輸液
200
5003
6ソリタ-T3号G輸液
200・500
3
フィジオゾール3号輸液
500
6
フルクトラクト注
200・500
6
ヴィーンD輸液
500
24
ハルトマン輸液「NP」
500
6
ポタコールR輸液
500
6
ラクテック注
250・500
6
ラクテックG輸液
500
3
2. 禁忌(次の患者には投与しないこと)
- 2.1 本剤の成分に対し過敏症の既往歴のある患者[9.1.1 参照]
- 2.2 バルプロ酸ナトリウム投与中の患者[10.1 参照]
4. 効能又は効果
-
一般感染症
-
〈適応菌種〉
メロペネムに感性のブドウ球菌属、レンサ球菌属、肺炎球菌、腸球菌属、髄膜炎菌、モラクセラ(ブランハメラ)・カタラーリス、大腸菌、シトロバクター属、クレブシエラ属、エンテロバクター属、セラチア属、プロテウス属、プロビデンシア属、インフルエンザ菌、シュードモナス属、緑膿菌、バークホルデリア・セパシア、バクテロイデス属、プレボテラ属
-
〈適応症〉
敗血症、深在性皮膚感染症、リンパ管・リンパ節炎、外傷・熱傷及び手術創等の二次感染、肛門周囲膿瘍、骨髄炎、関節炎、扁桃炎(扁桃周囲膿瘍を含む)、肺炎、肺膿瘍、膿胸、慢性呼吸器病変の二次感染、複雑性膀胱炎、腎盂腎炎、腹膜炎、胆嚢炎、胆管炎、肝膿瘍、子宮内感染、子宮付属器炎、子宮旁結合織炎、化膿性髄膜炎、眼内炎(全眼球炎を含む)、中耳炎、副鼻腔炎、顎骨周辺の蜂巣炎、顎炎
-
〈適応菌種〉
- 発熱性好中球減少症
5. 効能又は効果に関連する注意
-
〈効能共通〉
- 5.1 本剤投与前に感受性の確認が行えなかった場合、本剤投与開始後3日を目安として本剤に対する感受性を確認し、本剤投与が適正であるか判断すること。なお、本剤に感受性が認められない場合、速やかに他の薬剤に変更すること。[8.3 参照]
-
〈扁桃炎(扁桃周囲膿瘍を含む)、中耳炎、副鼻腔炎〉
- 5.2 「抗微生物薬適正使用の手引き」1) を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
-
〈発熱性好中球減少症〉
- 5.3 本剤は、以下の2条件を満たす症例に投与すること。
- 5.4 国内外のガイドライン等を参照し、本疾患の治療に十分な経験を持つ医師のもとで、本剤の使用が適切と判断される症例についてのみ実施すること。
- 5.5 本剤投与前に血液培養等の検査を実施すること。起炎菌が判明した際には、本剤投与継続の必要性を検討すること。
- 5.6 本剤投与の開始時期の指標である好中球数が緊急時等で確認できない場合には、白血球数の半数を好中球数として推定すること。
- 5.7 好中球数、発熱の回復が認められた場合には、本剤の投与中止を考慮すること。
- 5.8 腫瘍熱・薬剤熱等の非感染性の発熱であることが確認された場合には、速やかに本剤の投与を中止すること。
6. 用法及び用量
-
〈効能共通〉
本剤の使用に際しては、投与開始後3日を目安としてさらに継続投与が必要か判定し、投与中止又はより適切な他剤に切り替えるべきか検討を行うこと。
- 〈一般感染症〉
-
化膿性髄膜炎以外の一般感染症
通常、成人にはメロペネムとして、1日0.5~1g(力価)を2~3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜増減するが、重症・難治性感染症には、1回1g(力価)を上限として、1日3g(力価)まで増量することができる。
通常、小児にはメロペネムとして、1日30~60mg(力価)/kgを3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜増減するが、重症・難治性感染症には、1日120mg(力価)/kgまで増量することができる。ただし、成人における1日最大用量3g(力価)を超えないこととする。 -
化膿性髄膜炎
通常、成人にはメロペネムとして、1日6g(力価)を3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜減量する。
通常、小児にはメロペネムとして、1日120mg(力価)/kgを3回に分割し、30分以上かけて点滴静注する。なお、年齢・症状に応じて適宜減量する。ただし、成人における1日用量6g(力価)を超えないこととする。 -
〈発熱性好中球減少症〉
通常、成人にはメロペネムとして、1日3g(力価)を3回に分割し、30分以上かけて点滴静注する。
通常、小児にはメロペネムとして、1日120mg(力価)/kgを3回に分割し、30分以上かけて点滴静注する。ただし、成人における1日用量3g(力価)を超えないこととする。
7. 用法及び用量に関連する注意
-
7.1 腎機能障害のある患者では、次表を目安に本剤の投与量及び投与間隔を調節するなど、患者の状態を観察しながら慎重に投与すること。[9.2 参照],[16.6.1 参照]
Ccr※が50mL/min以下の腎機能障害患者(成人)の投与量、投与間隔の目安 Ccr(mL/min)
投与量、投与間隔
26~50
1回あたりの投与量を減量せず
12時間ごとに投与10~25
1回あたりの投与量を1/2に減量し
12時間ごとに投与<10
1回あたりの投与量を1/2に減量し
24時間ごとに投与※クレアチニンクリアランス
- 7.2 血液透析日には、透析終了後に投与すること。[13.1 参照]
8. 重要な基本的注意
-
8.1 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.1 参照]
- 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。[9.1.1 参照]
- 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
- 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
- 8.2 投与後3~5日目までは発疹等の副作用の発現には特に注意し、症状が発現したときには、他剤に切り替えるなど適切な処置を講じること。なお、継続使用にあたっても、引き続き副作用症状に注意すること。[11.1.7 参照]
- 8.3 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。[5.1 参照]
- 8.4 患者の状態から判断して、やむを得ず原因菌不明のまま本剤を使用した場合、数日間以内に改善の徴候が認められないときには、他剤に切り替えるなど適切な処置を講じること。なお、継続使用にあたっても、引き続き症状の改善等から判断し、漫然と長期の投与を行わないこと。
- 8.5 患者の状態等から判断して、7日以上にわたって本剤を投与する場合には、その理由を常時明確にし、発疹の出現や肝機能異常等の副作用に留意し、漫然とした継続投与は行わないこと。
- 8.6 AST、ALTの上昇があらわれることがあるので、1週間以上の使用に際しては、必ず肝機能検査を実施すること。
- 8.7 急性腎障害等の重篤な腎機能障害、劇症肝炎、肝機能障害、黄疸、汎血球減少、無顆粒球症、溶血性貧血、白血球減少、血小板減少があらわれることがあるので、定期的に臨床検査(腎機能検査、肝機能検査、血液検査等)を行うこと。[11.1.2 参照],[11.1.3 参照],[11.1.8 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
- 9.1.1 カルバペネム系、ペニシリン系又はセフェム系抗生物質に対し過敏症の既往歴のある患者(ただし、本剤に対し過敏症の既往歴のある患者には投与しないこと)
- 9.1.2 本人又は両親、兄弟に気管支喘息、発疹、じん麻疹等のアレルギー症状を起こしやすい体質を有する患者
-
9.1.3 経口摂取の不良な患者又は非経口栄養の患者、全身状態の悪い患者
ビタミンK欠乏症状があらわれることがある。
-
9.1.4 てんかんの既往歴あるいは中枢神経障害を有する患者
痙攣、意識障害等の中枢神経症状が起こりやすい。[11.1.6 参照]
9.2 腎機能障害患者
痙攣、意識障害等の中枢神経症状が起こりやすい。[7.1 参照],[11.1.6 参照],[16.6.1 参照]
9.3 肝機能障害患者
-
9.3.1 高度の肝機能障害のある患者
肝機能障害が悪化するおそれがある。[11.1.3 参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒト母乳中へ移行することが報告されている2) 。
9.7 小児等
低出生体重児、新生児を対象とした臨床試験は実施していない。国内の小児臨床試験では、軽度のAST、ALT上昇が多く報告されている。
11. 副作用
11.1 重大な副作用
-
11.1.1 ショック、アナフィラキシー(いずれも0.1%未満)
呼吸困難、不快感、口内異常感、喘鳴、眩暈、便意、耳鳴、発汗、全身潮紅、血管浮腫、じん麻疹等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。[8.1 参照]
- 11.1.2 急性腎障害等の重篤な腎機能障害(0.1%未満)
- 11.1.3 劇症肝炎(頻度不明)、肝機能障害(0.1~5%未満)、黄疸(0.1%未満)
-
11.1.4 偽膜性大腸炎等の血便を伴う重篤な大腸炎(0.1%未満)
腹痛、頻回の下痢があらわれた場合には直ちに投与を中止するなど適切な処置を行うこと。
-
11.1.5 間質性肺炎、PIE症候群(いずれも0.1%未満)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多等があらわれた場合には投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
- 11.1.6 痙攣、意識障害等の中枢神経症状(0.1%未満)
- 11.1.7 **中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(0.1%未満)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、急性汎発性発疹性膿疱症(頻度不明)
- 11.1.8 汎血球減少、無顆粒球症、溶血性貧血(いずれも頻度不明)、白血球減少、血小板減少(いずれも0.1%未満)
- 11.1.9 血栓性静脈炎(頻度不明)
11.2 その他の副作用
0.1~5%未満 |
0.1%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹、発熱 |
じん麻疹、紅斑、そう痒、発赤 |
熱感 |
血液 |
顆粒球減少、好酸球増多、血小板減少又は増多、赤血球減少、ヘモグロビンの減少 |
好塩基球増多、リンパ球増多、好中球増多、単球増多、ヘマトクリットの減少、異型リンパ球出現 |
|
肝臓 |
AST、ALT、LDH、ALP、LAP、γ-GTP、ビリルビン、尿ウロビリノーゲンの上昇 |
黄疸、コリンエステラーゼ低下 |
|
腎臓 |
BUN、クレアチニンの上昇 |
尿中β2-マイクログロブリンの上昇、尿蛋白陽性 |
|
消化器 |
下痢 |
嘔気、嘔吐、腹痛 |
食欲不振 |
菌交代症 |
口内炎、カンジダ症 |
||
ビタミン欠乏症 |
ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
||
その他 |
血清カリウム上昇 |
頭痛、倦怠感、不穏、血清ナトリウム低下、血清カリウム低下、CK上昇、トリグリセリド増加、胸部不快感、血中尿酸減少又は増加、注射部位反応(炎症、疼痛、硬結等) |
ミオクローヌス、せん妄 |
13. 過量投与
-
13.1 処置
本剤は血液透析又は血液ろ過により除去される。[7.2 参照]
14. 適用上の注意
14.1 薬剤調製時の注意
- 14.1.1 本剤溶解時、溶液は無色から微黄色澄明を呈するが、色の濃淡は本剤の効力には影響しない。
- 14.1.2 溶解後は速やかに使用すること。なお、やむを得ず保存を必要とする場合でも、日局生理食塩液に溶解した場合、室温保存では6時間以内に、5℃保存では24時間以内に使用すること。[14.1.4 参照]
- 14.1.3 通常0.25g~2.0g(力価)当たり100mL以上の日局生理食塩液等に溶解する。ただし、注射用水は等張にならないので使用しないこと。
-
14.1.4 主な輸液との配合変化
0.5gバイアル製剤を、25±2℃で主な輸液に溶解したとき、本剤の残存力価が90%以上を示した時間は下表のとおりである。[14.1.2 参照]
輸 液
残存力価90%以上を示した時間
(hr)名 称
容量
(mL)生理食塩液
10
1006
245%ブドウ糖注射液
10
1003
6キリット注5%
500
6
果糖注射液5%
500
6
アクチット輸液
200
6
10%EL-3号輸液
500
6
KN3号輸液
200
5003
6ソリタ-T3号輸液
200
5003
6ソリタ-T3号G輸液
200・500
3
フィジオゾール3号輸液
500
6
フルクトラクト注
200・500
6
ヴィーンD輸液
500
24
ハルトマン輸液「NP」
500
6
ポタコールR輸液
500
6
ラクテック注
250・500
6
ラクテックG輸液
500
3