薬効分類名セファマイシン系抗生物質製剤
一般的名称注射用セフメタゾールナトリウム
セフメタゾールNa静注用0.25g「NP」、セフメタゾールNa静注用0.5g「NP」、セフメタゾールNa静注用1g「NP」、セフメタゾールNa静注用2g「NP」、セフメタゾールナトリウム点滴静注用バッグ1g「NP」、セフメタゾールナトリウム点滴静注用バッグ2g「NP」
せふめたぞーるNaじょうちゅうよう0.25g「NP」、せふめたぞーるNaじょうちゅうよう0.5g「NP」、せふめたぞーるNaじょうちゅうよう1g「NP」、せふめたぞーるNaじょうちゅうよう2g「NP」、せふめたぞーるなとりうむてんてきじょうちゅうようばっぐ1g「NP」、せふめたぞーるなとりうむてんてきじょうちゅうようばっぐ2g「NP」
Cefmetazole Sodium for Intravenous, Cefmetazole Sodium for Intravenous, Cefmetazole Sodium for Intravenous, Cefmetazole Sodium for Intravenous, Cefmetazole Sodium for I.V. Infusion, Cefmetazole Sodium for I.V. Infusion
製造販売元/ニプロ株式会社
重大な副作用
その他の副作用
併用注意
アルコール
飲酒により、ジスルフィラム様作用(顔面潮紅、心悸亢進、めまい、頭痛、嘔気等)があらわれることがある。投与期間中及び投与後少なくとも1週間は飲酒を避けさせること。
明らかではないが、3位側鎖のN-メチルチオテトラゾール基がジスルフィラム様作用を有すると考えられている。
利尿剤
- フロセミド等
腎障害が増強されるおそれがある。
機序は不明だが、動物実験(ラット)でフロセミドとの併用により、軽度から中等度の近位尿細管上皮細胞の核の萎縮及び濃縮が認められたとの報告がある。
2. 禁忌(次の患者には投与しないこと)
本剤の成分に対し過敏症の既往歴のある患者
5. 効能・効果に関連する注意
-
〈急性気管支炎〉
「抗微生物薬適正使用の手引き」1) を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
6. 用法・用量
-
〈バイアル〉
通常成人には、1日1~2g(力価)を2回に分けて静脈内注射または点滴静注する。
通常小児には、1日25~100mg(力価)/kgを2~4回に分けて静脈内注射または点滴静注する。
なお、難治性または重症感染症には症状に応じて、1日量を成人では4g(力価)、小児では150mg(力価)/kgまで増量し、2~4回に分割投与する。
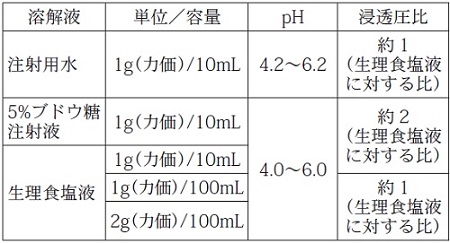
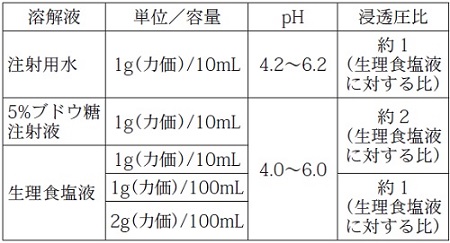
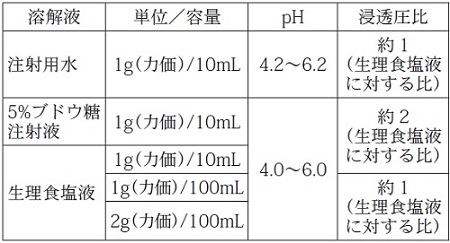
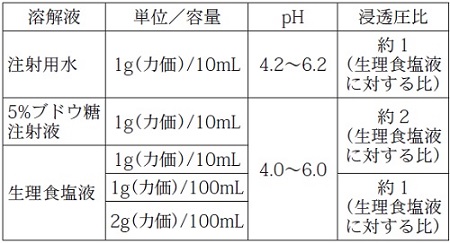
静脈内注射に際しては、本剤1g(力価)当たり、日本薬局方注射用水、日本薬局方生理食塩液または日本薬局方ブドウ糖注射液10mLに溶解し、緩徐に投与する。なお、本剤は補液に加えて点滴静注することもできる。 -
〈バッグ〉
通常成人には、1日1~2g(力価)を2回に分けて静脈内注射または点滴静注する。
通常小児には、1日25~100mg(力価)/kgを2~4回に分けて静脈内注射または点滴静注する。
なお、難治性または重症感染症には症状に応じて、1日量を成人では4g(力価)、小児では150mg(力価)/kgまで増量し、2~4回に分割投与する。
用時添付の生理食塩液に溶解し、緩徐に投与する。なお、本剤は補液に加えて点滴静注することもできる。
8. 重要な基本的注意
- 8.1 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
- 8.2 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、以下の措置をとること。[11.1.1 参照]
- 8.3 急性腎障害等の重篤な腎障害があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[11.1.3 参照]
- 8.4 投与に際しては、定期的に肝機能、血液等の検査を行うことが望ましい。[11.1.4 参照],[11.1.5 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.2 腎機能障害患者
-
〈製剤共通〉
-
9.2.1 高度の腎障害のある患者
投与量・投与間隔の適切な調節をするなど慎重に投与すること。血中濃度の上昇、半減期の延長がみられることがある。[16.6.1 参照]
-
9.2.1 高度の腎障害のある患者
- 〈バッグ〉
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
11. 副作用
11.1 重大な副作用
-
11.1.1 ショック(0.01%未満)、アナフィラキシー(頻度不明)
ショック、アナフィラキシー(不快感、口内異常感、喘鳴、眩暈、便意、耳鳴、発汗等)を起こすことがある。[8.2 参照]
- 11.1.2 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(いずれも頻度不明)
-
11.1.3 急性腎障害(頻度不明)
急性腎障害等の重篤な腎障害があらわれることがあるので、観察を十分に行い、BUN・血中クレアチニン上昇等の検査所見があらわれた場合には直ちに投与を中止し、適切な処置を行うこと。[8.3 参照]
-
11.1.4 肝炎、肝機能障害、黄疸(いずれも頻度不明)
AST、ALTの著しい上昇等を伴う肝炎、肝機能障害、黄疸があらわれることがある。[8.4 参照]
- 11.1.5 無顆粒球症、溶血性貧血、血小板減少(いずれも頻度不明)
-
11.1.6 偽膜性大腸炎(0.01%未満)
偽膜性大腸炎等の血便を伴う重篤な大腸炎(初期症状:腹痛、頻回の下痢)があらわれることがある。
-
11.1.7 間質性肺炎、PIE症候群(いずれも頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多等を伴う間質性肺炎、PIE症候群があらわれることがあるので、このような症状があらわれた場合には直ちに投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.2 その他の副作用
0.1~1%未満 |
0.1%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹、そう痒 |
蕁麻疹、紅斑、発熱 |
- |
血液 |
顆粒球減少、好酸球増多 |
赤血球減少、血小板減少 |
- |
肝臓 |
AST上昇、ALT上昇、肝機能異常 |
ALP上昇 |
- |
消化器 |
悪心・嘔吐、下痢 |
食欲不振 |
- |
菌交代症 |
- |
口内炎、カンジダ症 |
- |
ビタミン欠乏症 |
- |
ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等) |
その他 |
- |
頭痛 |
- |
2. 禁忌(次の患者には投与しないこと)
本剤の成分に対し過敏症の既往歴のある患者
5. 効能・効果に関連する注意
-
〈急性気管支炎〉
「抗微生物薬適正使用の手引き」1) を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
6. 用法・用量
-
〈バイアル〉
通常成人には、1日1~2g(力価)を2回に分けて静脈内注射または点滴静注する。
通常小児には、1日25~100mg(力価)/kgを2~4回に分けて静脈内注射または点滴静注する。
なお、難治性または重症感染症には症状に応じて、1日量を成人では4g(力価)、小児では150mg(力価)/kgまで増量し、2~4回に分割投与する。
静脈内注射に際しては、本剤1g(力価)当たり、日本薬局方注射用水、日本薬局方生理食塩液または日本薬局方ブドウ糖注射液10mLに溶解し、緩徐に投与する。なお、本剤は補液に加えて点滴静注することもできる。 -
〈バッグ〉
通常成人には、1日1~2g(力価)を2回に分けて静脈内注射または点滴静注する。
通常小児には、1日25~100mg(力価)/kgを2~4回に分けて静脈内注射または点滴静注する。
なお、難治性または重症感染症には症状に応じて、1日量を成人では4g(力価)、小児では150mg(力価)/kgまで増量し、2~4回に分割投与する。
用時添付の生理食塩液に溶解し、緩徐に投与する。なお、本剤は補液に加えて点滴静注することもできる。
8. 重要な基本的注意
- 8.1 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
- 8.2 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、以下の措置をとること。[11.1.1 参照]
- 8.3 急性腎障害等の重篤な腎障害があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[11.1.3 参照]
- 8.4 投与に際しては、定期的に肝機能、血液等の検査を行うことが望ましい。[11.1.4 参照],[11.1.5 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.2 腎機能障害患者
-
〈製剤共通〉
-
9.2.1 高度の腎障害のある患者
投与量・投与間隔の適切な調節をするなど慎重に投与すること。血中濃度の上昇、半減期の延長がみられることがある。[16.6.1 参照]
-
9.2.1 高度の腎障害のある患者
- 〈バッグ〉
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
11. 副作用
11.1 重大な副作用
-
11.1.1 ショック(0.01%未満)、アナフィラキシー(頻度不明)
ショック、アナフィラキシー(不快感、口内異常感、喘鳴、眩暈、便意、耳鳴、発汗等)を起こすことがある。[8.2 参照]
- 11.1.2 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(いずれも頻度不明)
-
11.1.3 急性腎障害(頻度不明)
急性腎障害等の重篤な腎障害があらわれることがあるので、観察を十分に行い、BUN・血中クレアチニン上昇等の検査所見があらわれた場合には直ちに投与を中止し、適切な処置を行うこと。[8.3 参照]
-
11.1.4 肝炎、肝機能障害、黄疸(いずれも頻度不明)
AST、ALTの著しい上昇等を伴う肝炎、肝機能障害、黄疸があらわれることがある。[8.4 参照]
- 11.1.5 無顆粒球症、溶血性貧血、血小板減少(いずれも頻度不明)
-
11.1.6 偽膜性大腸炎(0.01%未満)
偽膜性大腸炎等の血便を伴う重篤な大腸炎(初期症状:腹痛、頻回の下痢)があらわれることがある。
-
11.1.7 間質性肺炎、PIE症候群(いずれも頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多等を伴う間質性肺炎、PIE症候群があらわれることがあるので、このような症状があらわれた場合には直ちに投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.2 その他の副作用
0.1~1%未満 |
0.1%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹、そう痒 |
蕁麻疹、紅斑、発熱 |
- |
血液 |
顆粒球減少、好酸球増多 |
赤血球減少、血小板減少 |
- |
肝臓 |
AST上昇、ALT上昇、肝機能異常 |
ALP上昇 |
- |
消化器 |
悪心・嘔吐、下痢 |
食欲不振 |
- |
菌交代症 |
- |
口内炎、カンジダ症 |
- |
ビタミン欠乏症 |
- |
ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等) |
その他 |
- |
頭痛 |
- |