薬効分類名アミノグリコシド系抗生物質製剤
一般的名称アミカシン硫酸塩
アミカシン硫酸塩注射液100mg「明治」、アミカシン硫酸塩注射液200mg「明治」
あみかしんりゅうさんえんちゅうしゃえき100mg「めいじ」、あみかしんりゅうさんえんちゅうしゃえき200mg「めいじ」
AMIKACIN SULFATE Injection「MEIJI」, AMIKACIN SULFATE Injection「MEIJI」
製造販売元/Meiji Seika ファルマ株式会社
重大な副作用
その他の副作用
併用注意
腎障害を起こすおそれのある血液代用剤
- デキストラン
ヒドロキシエチルデンプン 等
腎障害が発現、悪化することがあるので、併用は避けることが望ましい。
機序は明確でないが、併用によりアミノグリコシド系抗生物質の血中への蓄積、近位尿細管上皮の空胞変性が生じるという報告がある。
ループ利尿剤
- フロセミド
アゾセミド - トラセミド 等
腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。
機序は明確でないが、併用によりアミノグリコシド系抗生物質の血中濃度の上昇、腎への蓄積が起こるという報告がある。
腎毒性及び聴器毒性を有する薬剤
- バンコマイシン塩酸塩
エンビオマイシン硫酸塩
白金含有抗悪性腫瘍剤(シスプラチン、カルボプラチン、ネダプラチン) 等
腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。
両薬剤ともに腎毒性、聴器毒性を有するが、相互作用の機序は不明。
麻酔剤
筋弛緩剤
- ロクロニウム臭化物
A型ボツリヌス毒素製剤 等
コリスチンメタンスルホン酸ナトリウム
呼吸抑制があらわれるおそれがある。呼吸抑制があらわれた場合には必要に応じ、コリンエステラーゼ阻害剤、カルシウム製剤の投与等の適切な処置を行うこと。
両薬剤ともに神経筋遮断作用を有しており、併用によりその作用が増強される。
腎毒性を有する薬剤
- シクロスポリン
アムホテリシンB 等
腎障害が発現、悪化するおそれがある。
両薬剤ともに腎毒性を有するが、相互作用の機序は不明。
2. 禁忌(次の患者には投与しないこと)
本剤の成分並びにアミノグリコシド系抗生物質又はバシトラシンに対し過敏症の既往歴のある患者[8.1.1 参照]
6. 用法・用量
-
〈筋肉内投与の場合〉
通常、成人1回アミカシン硫酸塩として100~200mg(力価)を1日1~2回筋肉内投与する。小児は、アミカシン硫酸塩として1日4~8mg(力価)/kgとし、1日1~2回筋肉内投与する。
なお、年齢及び症状により適宜増減する。 -
〈点滴静脈内投与の場合〉
通常、成人1回アミカシン硫酸塩として100~200mg(力価)を、1日2回点滴静脈内投与する。小児はアミカシン硫酸塩として1日4~8mg(力価)/kgとし、1日2回点滴静脈内投与する。また、新生児(未熟児を含む)は、1回アミカシン硫酸塩として6mg(力価)/kgを、1日2回点滴静脈内投与する。
なお、年齢、体重及び症状により適宜増減する。
点滴静脈内投与の場合には、通常100~500mLの補液中に100~200mg(力価)の割合で溶解し、30分~1時間かけて投与すること。
7. 用法・用量に関連する注意
腎障害患者では、起炎菌の感受性、感染症の重症度、感染部位、腎機能障害の程度を考慮に入れ、投与量・投与間隔を調整すること。[8.2 参照],[9.2 参照],[16.6.1 参照],[16.8.1 参照]
-
7.1 1回投与量を調節する方法
体重及びクレアチニン・クリアランスを用い、図1又は計算式より求めた初回量及び維持量を投与する1) 。
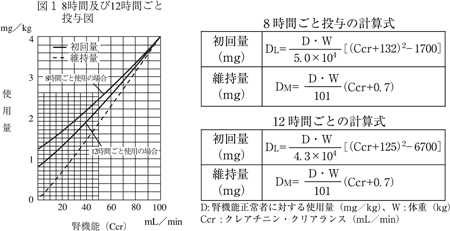
-
7.2 投与間隔を調節する方法
「血清クレアチニン値×9」時間ごとに通常量を投与する。
8. 重要な基本的注意
-
8.1 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.1 参照]
- 8.1.1 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。[2 参照]
- 8.1.2 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
- 8.1.3 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
- 8.2 眩暈、耳鳴、難聴等の第8脳神経障害があらわれることがあるので慎重に投与すること。特に腎機能障害患者、高齢者、長期間投与患者及び大量投与患者等では血中濃度が高くなりやすく、聴力障害の危険性がより大きくなるので、聴力検査を実施することが望ましい。アミノグリコシド系抗生物質の聴力障害は、高周波音に始まり低周波音へと波及するので、障害の早期発見のために、聴力検査の最高周波数である8kHzでの検査が有用である。[7 参照],[9.2 参照],[9.8.1 参照],[11.1.2 参照],[16.6.1 参照],[16.8.1 参照]
- 8.3 急性腎障害等の重篤な腎障害があらわれることがあるので、定期的に検査を実施するなど観察を十分に行うこと。[9.8.1 参照],[11.1.3 参照],[16.8.1 参照]
- 8.4 投与後は血中濃度をモニタリングすることが望ましい。[16.8.1 参照]
- 8.5 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.2 腎機能障害患者
投与量を減らすか、投与間隔をあけて投与すること。高い血中濃度が持続し、腎障害が悪化するおそれがあり、また、第8脳神経障害等の副作用が強くあらわれるおそれがある。[7 参照],[8.2 参照],[16.6.1 参照],[16.8.1 参照]
9.3 肝機能障害患者
肝障害を悪化させるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。アミカシン硫酸塩はヒト胎盤を通過する。新生児に第8脳神経障害があらわれるおそれがある。[16.3.1 参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.8 高齢者
次の点に注意し、用量並びに投与間隔に留意するなど患者の状態を観察しながら慎重に投与すること。
- 9.8.1 本剤は主として腎臓から排泄されるが、高齢者では腎機能が低下していることが多いため、高い血中濃度が持続するおそれがあり、第8脳神経障害、腎障害等の副作用があらわれやすい。[8.2 参照],[8.3 参照],[16.8.1 参照]
- 9.8.2 ビタミンK欠乏による出血傾向があらわれることがある。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
腎障害が発現、悪化することがあるので、併用は避けることが望ましい。 腎障害が発生した場合には、投与を中止し、透析療法等適切な処置を行うこと。 |
機序は明確でないが、併用によりアミノグリコシド系抗生物質の血中への蓄積、近位尿細管上皮の空胞変性が生じるという報告がある。 |
|
腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。 |
機序は明確でないが、併用によりアミノグリコシド系抗生物質の血中濃度の上昇、腎への蓄積が起こるという報告がある。 |
|
腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。 |
両薬剤ともに腎毒性、聴器毒性を有するが、相互作用の機序は不明。 |
|
呼吸抑制があらわれるおそれがある。呼吸抑制があらわれた場合には必要に応じ、コリンエステラーゼ阻害剤、カルシウム製剤の投与等の適切な処置を行うこと。 |
両薬剤ともに神経筋遮断作用を有しており、併用によりその作用が増強される。 |
|
腎障害が発現、悪化するおそれがある。 |
両薬剤ともに腎毒性を有するが、相互作用の機序は不明。 |
11. 副作用
11.1 重大な副作用
11.2 その他の副作用
0.1~5%未満 |
0.1%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹 |
そう痒、発熱 |
|
腎臓 |
浮腫、蛋白尿、血尿、血清クレアチニン上昇、BUN上昇、乏尿 |
カリウム等の電解質異常 |
|
肝臓 |
AST上昇、ALT上昇 |
Al-P上昇 |
|
血液 |
白血球減少、好酸球増多 |
||
消化器 |
下痢、悪心・嘔吐 |
||
ビタミン欠乏症 |
ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
||
投与部位 (筋注の場合) |
注射部位の疼痛、硬結 |
||
その他 |
頭痛、口唇部のしびれ感 |
2. 禁忌(次の患者には投与しないこと)
本剤の成分並びにアミノグリコシド系抗生物質又はバシトラシンに対し過敏症の既往歴のある患者[8.1.1 参照]
6. 用法・用量
-
〈筋肉内投与の場合〉
通常、成人1回アミカシン硫酸塩として100~200mg(力価)を1日1~2回筋肉内投与する。小児は、アミカシン硫酸塩として1日4~8mg(力価)/kgとし、1日1~2回筋肉内投与する。
なお、年齢及び症状により適宜増減する。 -
〈点滴静脈内投与の場合〉
通常、成人1回アミカシン硫酸塩として100~200mg(力価)を、1日2回点滴静脈内投与する。小児はアミカシン硫酸塩として1日4~8mg(力価)/kgとし、1日2回点滴静脈内投与する。また、新生児(未熟児を含む)は、1回アミカシン硫酸塩として6mg(力価)/kgを、1日2回点滴静脈内投与する。
なお、年齢、体重及び症状により適宜増減する。
点滴静脈内投与の場合には、通常100~500mLの補液中に100~200mg(力価)の割合で溶解し、30分~1時間かけて投与すること。
7. 用法・用量に関連する注意
腎障害患者では、起炎菌の感受性、感染症の重症度、感染部位、腎機能障害の程度を考慮に入れ、投与量・投与間隔を調整すること。[8.2 参照],[9.2 参照],[16.6.1 参照],[16.8.1 参照]
-
7.1 1回投与量を調節する方法
体重及びクレアチニン・クリアランスを用い、図1又は計算式より求めた初回量及び維持量を投与する1) 。

-
7.2 投与間隔を調節する方法
「血清クレアチニン値×9」時間ごとに通常量を投与する。
8. 重要な基本的注意
-
8.1 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.1 参照]
- 8.1.1 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。[2 参照]
- 8.1.2 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
- 8.1.3 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
- 8.2 眩暈、耳鳴、難聴等の第8脳神経障害があらわれることがあるので慎重に投与すること。特に腎機能障害患者、高齢者、長期間投与患者及び大量投与患者等では血中濃度が高くなりやすく、聴力障害の危険性がより大きくなるので、聴力検査を実施することが望ましい。アミノグリコシド系抗生物質の聴力障害は、高周波音に始まり低周波音へと波及するので、障害の早期発見のために、聴力検査の最高周波数である8kHzでの検査が有用である。[7 参照],[9.2 参照],[9.8.1 参照],[11.1.2 参照],[16.6.1 参照],[16.8.1 参照]
- 8.3 急性腎障害等の重篤な腎障害があらわれることがあるので、定期的に検査を実施するなど観察を十分に行うこと。[9.8.1 参照],[11.1.3 参照],[16.8.1 参照]
- 8.4 投与後は血中濃度をモニタリングすることが望ましい。[16.8.1 参照]
- 8.5 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.2 腎機能障害患者
投与量を減らすか、投与間隔をあけて投与すること。高い血中濃度が持続し、腎障害が悪化するおそれがあり、また、第8脳神経障害等の副作用が強くあらわれるおそれがある。[7 参照],[8.2 参照],[16.6.1 参照],[16.8.1 参照]
9.3 肝機能障害患者
肝障害を悪化させるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。アミカシン硫酸塩はヒト胎盤を通過する。新生児に第8脳神経障害があらわれるおそれがある。[16.3.1 参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.8 高齢者
次の点に注意し、用量並びに投与間隔に留意するなど患者の状態を観察しながら慎重に投与すること。
- 9.8.1 本剤は主として腎臓から排泄されるが、高齢者では腎機能が低下していることが多いため、高い血中濃度が持続するおそれがあり、第8脳神経障害、腎障害等の副作用があらわれやすい。[8.2 参照],[8.3 参照],[16.8.1 参照]
- 9.8.2 ビタミンK欠乏による出血傾向があらわれることがある。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
腎障害が発現、悪化することがあるので、併用は避けることが望ましい。 腎障害が発生した場合には、投与を中止し、透析療法等適切な処置を行うこと。 |
機序は明確でないが、併用によりアミノグリコシド系抗生物質の血中への蓄積、近位尿細管上皮の空胞変性が生じるという報告がある。 |
|
腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。 |
機序は明確でないが、併用によりアミノグリコシド系抗生物質の血中濃度の上昇、腎への蓄積が起こるという報告がある。 |
|
腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。 |
両薬剤ともに腎毒性、聴器毒性を有するが、相互作用の機序は不明。 |
|
呼吸抑制があらわれるおそれがある。呼吸抑制があらわれた場合には必要に応じ、コリンエステラーゼ阻害剤、カルシウム製剤の投与等の適切な処置を行うこと。 |
両薬剤ともに神経筋遮断作用を有しており、併用によりその作用が増強される。 |
|
腎障害が発現、悪化するおそれがある。 |
両薬剤ともに腎毒性を有するが、相互作用の機序は不明。 |
11. 副作用
11.1 重大な副作用
11.2 その他の副作用
0.1~5%未満 |
0.1%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹 |
そう痒、発熱 |
|
腎臓 |
浮腫、蛋白尿、血尿、血清クレアチニン上昇、BUN上昇、乏尿 |
カリウム等の電解質異常 |
|
肝臓 |
AST上昇、ALT上昇 |
Al-P上昇 |
|
血液 |
白血球減少、好酸球増多 |
||
消化器 |
下痢、悪心・嘔吐 |
||
ビタミン欠乏症 |
ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
||
投与部位 (筋注の場合) |
注射部位の疼痛、硬結 |
||
その他 |
頭痛、口唇部のしびれ感 |