薬効分類名グリコペプチド系抗生物質製剤
一般的名称バンコマイシン塩酸塩
バンコマイシン塩酸塩点滴静注用0.5g「VTRS」、バンコマイシン塩酸塩点滴静注用1g「VTRS」
ばんこまいしんえんさんえんてんてきじょうちゅうよう0.5g「VTRS」、ばんこまいしんえんさんえんてんてきじょうちゅうよう1g「VTRS」
VANCOMYCIN Hydrochloride for Injection, VANCOMYCIN Hydrochloride for Injection
製造販売元/ヴィアトリス・ヘルスケア合同会社、販売元/ヴィアトリス製薬合同会社
重大な副作用
その他の副作用
併用注意
- 全身麻酔薬
同時に投与すると、紅斑、ヒスタミン様潮紅、アナフィラキシー反応等の副作用が発現することがある。
全身麻酔の開始1時間前には本剤の点滴静注を終了すること。
全身麻酔薬には、アナフィラキシー作用、ヒスタミン遊離作用を有するものがあり、本剤にもヒスタミン遊離作用がある。しかし、相互作用の機序は不明である。
- 腎毒性及び聴器毒性を有する薬剤
- [8.3 参照],[16.6.1 参照]
腎障害、聴覚障害が発現、悪化するおそれがあるので、併用は避けること。やむを得ず併用する場合は、慎重に投与すること。
機序:両剤共に腎毒性、聴器毒性を有するが、相互作用の機序は不明である。
危険因子:腎障害のある患者、高齢者、長期投与の患者等
- 腎毒性を有する薬剤
- [8.3 参照],[16.6.1 参照]
腎障害が発現、悪化するおそれがあるので、併用は避けること。やむを得ず併用する場合は、慎重に投与すること。
機序:両剤共に腎毒性を有するが、相互作用の機序は不明である。
危険因子:腎障害のある患者、高齢者、長期投与の患者等
1. 警告
本剤の耐性菌の発現を防ぐため、「5. 効能・効果に関連する注意」、「8. 重要な基本的注意」の項を熟読の上、適正使用に努めること。
2. 禁忌(次の患者には投与しないこと)
本剤の成分に対し過敏症の既往歴のある患者
5. 効能・効果に関連する注意
- 〈効能共通〉
-
〈化膿性髄膜炎〉
- 5.3 後遺症として聴覚障害が発現するおそれがあるので、特に小児等、適応患者の選択に十分注意し、慎重に投与すること。[11.1.6 参照]
- 〈PRSP肺炎〉
- 〈MRSA又はMRCNS感染が疑われる発熱性好中球減少症〉
6. 用法・用量
通常、成人にはバンコマイシン塩酸塩として1日2g(力価)を1回0.5g(力価)6時間ごと又は1回1g(力価)12時間ごとに分割して、それぞれ60分以上かけて点滴静注する。
なお、年齢、体重、症状により適宜増減する。
高齢者には、1回0.5g(力価)12時間ごと又は1回1g(力価)24時間ごとに、それぞれ60分以上かけて点滴静注する。
なお、年齢、体重、症状により適宜増減する。
小児、乳児には、1日40mg(力価)/kgを2~4回に分割して、それぞれ60分以上かけて点滴静注する。
新生児には、1回投与量を10~15mg(力価)/kgとし、生後1週までの新生児に対しては12時間ごと、生後1ヵ月までの新生児に対しては8時間ごとに、それぞれ60分以上かけて点滴静注する。
7. 用法・用量に関連する注意
-
〈効能共通〉
- 7.1 急速なワンショット静注又は短時間での点滴静注を行うとヒスタミンが遊離されてred neck(red man)症候群(顔、頸、躯幹の紅斑性充血、そう痒等)、血圧低下等の副作用が発現することがあるので、60分以上かけて点滴静注すること。
-
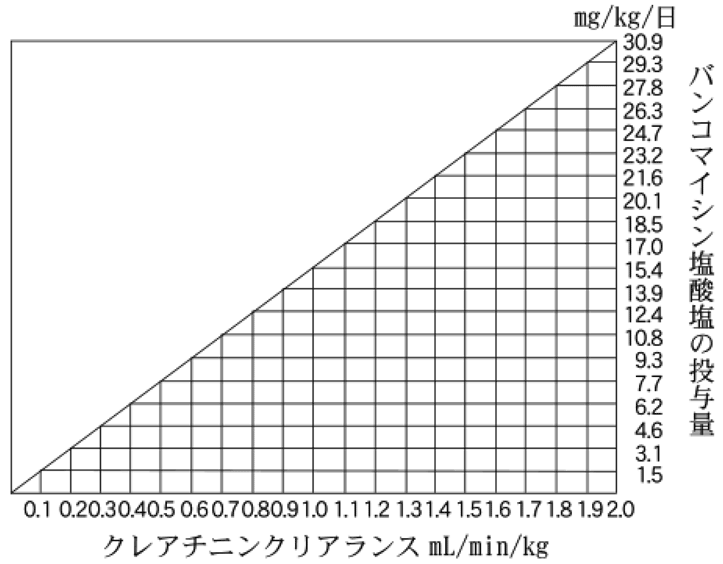
7.2 腎機能障害患者では健康者より血中濃度の半減期が延長するので、投与量を修正して使用する必要がある。クレアチニンクリアランスから投与量を修正する目安は下図により算出できる1)
(外国人データ)。[9.2 参照],[16.6.1 参照]
- 〈MRSA又はMRCNS感染が疑われる発熱性好中球減少症〉
8. 重要な基本的注意
- 8.1 本剤の使用にあたっては、耐性菌の発現を防ぐため、次のことに注意すること。
- 8.2 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.1 参照]
- 8.3 投与期間中は血中濃度をモニタリングすることが望ましい。[9.1.2 参照],[9.2 参照],[9.7 参照],[9.8 参照],[10.2 参照],[16.8.1 参照]
- 8.4 重篤な腎障害があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[11.1.2 参照]
- 8.5 第8脳神経障害があらわれることがあるので、聴力検査等観察を十分に行うこと。[11.1.6 参照]
- 8.6 肝機能障害、黄疸があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[11.1.8 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 テイコプラニン、ペプチド系抗生物質又はアミノグリコシド系抗生物質に対し過敏症の既往歴のある患者(ただし、バンコマイシンに対し過敏症のある患者には投与しないこと)
治療上やむを得ないと判断される場合を除き、投与しないこと。
-
9.1.2 ペプチド系抗生物質、アミノグリコシド系抗生物質、テイコプラニンによる難聴又はその他の難聴のある患者
治療上やむを得ないと判断される場合を除き、投与しないこと。難聴が発現又は増悪するおそれがある。[8.3 参照],[16.8.1 参照]
9.2 腎機能障害患者
腎機能障害の程度に応じた投与量・投与間隔の調節が必要となる。血中濃度をモニタリングするなど慎重に投与すること。排泄が遅延し、蓄積する。[7.2 参照],[8.3 参照],[16.6.1 参照],[16.8.1 参照]
9.3 肝機能障害患者
肝障害が悪化することがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
授乳しないことが望ましい。ヒト母乳中に移行する。
9.7 小児等
血中濃度をモニタリングするなど慎重に投与すること。腎の発達段階にあるため、特に低出生体重児、新生児においては血中濃度の半減期が延長し高い血中濃度が長時間持続するおそれがある。[8.3 参照],[16.6.2 参照],[16.6.3 参照],[16.8.1 参照]
9.8 高齢者
投与前及び投与中に腎機能検査を行い、腎機能低下の程度により投与量・投与間隔を調節し、血中濃度をモニタリングするなど慎重に投与すること。高齢者では腎機能が低下している場合が多い。[8.3 参照],[16.6.4 参照],[16.8.1 参照]
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
同時に投与すると、紅斑、ヒスタミン様潮紅、アナフィラキシー反応等の副作用が発現することがある。 |
全身麻酔薬には、アナフィラキシー作用、ヒスタミン遊離作用を有するものがあり、本剤にもヒスタミン遊離作用がある。しかし、相互作用の機序は不明である。 |
|
|
腎障害、聴覚障害が発現、悪化するおそれがあるので、併用は避けること。やむを得ず併用する場合は、慎重に投与すること。 |
機序:両剤共に腎毒性、聴器毒性を有するが、相互作用の機序は不明である。 |
|
腎障害が発現、悪化するおそれがあるので、併用は避けること。やむを得ず併用する場合は、慎重に投与すること。 |
機序:両剤共に腎毒性を有するが、相互作用の機序は不明である。 |
11. 副作用
11.1 重大な副作用
-
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
ショック、アナフィラキシー(呼吸困難、全身潮紅、浮腫等)を起こすことがある。[8.2 参照]
-
11.1.2 急性腎障害、間質性腎炎(いずれも頻度不明)
急性腎障害、間質性腎炎等の重篤な腎障害があらわれることがある。[8.4 参照]
- 11.1.3 汎血球減少、無顆粒球症、血小板減少(いずれも頻度不明)
- 11.1.4 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、剥脱性皮膚炎(いずれも頻度不明)
-
11.1.5 薬剤性過敏症症候群(頻度不明)
初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがある。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること2) 。
- 11.1.6 第8脳神経障害(頻度不明)
-
11.1.7 偽膜性大腸炎(頻度不明)
偽膜性大腸炎等の血便を伴う重篤な大腸炎があらわれることがあるので、腹痛、頻回の下痢があらわれた場合には、直ちに投与を中止するなど適切な処置を行うこと。
-
11.1.8 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、Al-P等の上昇、黄疸があらわれることがある。[8.6 参照]
11.2 その他の副作用
2%以上 |
2%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹 |
発赤、顔面潮紅 |
そう痒、蕁麻疹、線状IgA水疱症 |
肝臓 |
AST上昇、ALT上昇、ビリルビン上昇 |
Al-P上昇、LDH上昇 |
γ-GTP上昇、LAP上昇 |
腎臓 |
BUN上昇 |
クレアチニン上昇 |
|
血液 |
白血球減少、血小板減少、好酸球増多 |
貧血 |
|
消化器 |
下痢 |
嘔気、嘔吐、腹痛 |
|
その他 |
発熱、静脈炎、血管痛 |
皮膚血管炎、悪寒、注射部疼痛 |
1. 警告
本剤の耐性菌の発現を防ぐため、「5. 効能・効果に関連する注意」、「8. 重要な基本的注意」の項を熟読の上、適正使用に努めること。
2. 禁忌(次の患者には投与しないこと)
本剤の成分に対し過敏症の既往歴のある患者
5. 効能・効果に関連する注意
- 〈効能共通〉
-
〈化膿性髄膜炎〉
- 5.3 後遺症として聴覚障害が発現するおそれがあるので、特に小児等、適応患者の選択に十分注意し、慎重に投与すること。[11.1.6 参照]
- 〈PRSP肺炎〉
- 〈MRSA又はMRCNS感染が疑われる発熱性好中球減少症〉
6. 用法・用量
通常、成人にはバンコマイシン塩酸塩として1日2g(力価)を1回0.5g(力価)6時間ごと又は1回1g(力価)12時間ごとに分割して、それぞれ60分以上かけて点滴静注する。
なお、年齢、体重、症状により適宜増減する。
高齢者には、1回0.5g(力価)12時間ごと又は1回1g(力価)24時間ごとに、それぞれ60分以上かけて点滴静注する。
なお、年齢、体重、症状により適宜増減する。
小児、乳児には、1日40mg(力価)/kgを2~4回に分割して、それぞれ60分以上かけて点滴静注する。
新生児には、1回投与量を10~15mg(力価)/kgとし、生後1週までの新生児に対しては12時間ごと、生後1ヵ月までの新生児に対しては8時間ごとに、それぞれ60分以上かけて点滴静注する。
7. 用法・用量に関連する注意
-
〈効能共通〉
- 7.1 急速なワンショット静注又は短時間での点滴静注を行うとヒスタミンが遊離されてred neck(red man)症候群(顔、頸、躯幹の紅斑性充血、そう痒等)、血圧低下等の副作用が発現することがあるので、60分以上かけて点滴静注すること。
-
7.2 腎機能障害患者では健康者より血中濃度の半減期が延長するので、投与量を修正して使用する必要がある。クレアチニンクリアランスから投与量を修正する目安は下図により算出できる1)
(外国人データ)。[9.2 参照],[16.6.1 参照]

- 〈MRSA又はMRCNS感染が疑われる発熱性好中球減少症〉
8. 重要な基本的注意
- 8.1 本剤の使用にあたっては、耐性菌の発現を防ぐため、次のことに注意すること。
- 8.2 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.1 参照]
- 8.3 投与期間中は血中濃度をモニタリングすることが望ましい。[9.1.2 参照],[9.2 参照],[9.7 参照],[9.8 参照],[10.2 参照],[16.8.1 参照]
- 8.4 重篤な腎障害があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[11.1.2 参照]
- 8.5 第8脳神経障害があらわれることがあるので、聴力検査等観察を十分に行うこと。[11.1.6 参照]
- 8.6 肝機能障害、黄疸があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[11.1.8 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 テイコプラニン、ペプチド系抗生物質又はアミノグリコシド系抗生物質に対し過敏症の既往歴のある患者(ただし、バンコマイシンに対し過敏症のある患者には投与しないこと)
治療上やむを得ないと判断される場合を除き、投与しないこと。
-
9.1.2 ペプチド系抗生物質、アミノグリコシド系抗生物質、テイコプラニンによる難聴又はその他の難聴のある患者
治療上やむを得ないと判断される場合を除き、投与しないこと。難聴が発現又は増悪するおそれがある。[8.3 参照],[16.8.1 参照]
9.2 腎機能障害患者
腎機能障害の程度に応じた投与量・投与間隔の調節が必要となる。血中濃度をモニタリングするなど慎重に投与すること。排泄が遅延し、蓄積する。[7.2 参照],[8.3 参照],[16.6.1 参照],[16.8.1 参照]
9.3 肝機能障害患者
肝障害が悪化することがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
授乳しないことが望ましい。ヒト母乳中に移行する。
9.7 小児等
血中濃度をモニタリングするなど慎重に投与すること。腎の発達段階にあるため、特に低出生体重児、新生児においては血中濃度の半減期が延長し高い血中濃度が長時間持続するおそれがある。[8.3 参照],[16.6.2 参照],[16.6.3 参照],[16.8.1 参照]
9.8 高齢者
投与前及び投与中に腎機能検査を行い、腎機能低下の程度により投与量・投与間隔を調節し、血中濃度をモニタリングするなど慎重に投与すること。高齢者では腎機能が低下している場合が多い。[8.3 参照],[16.6.4 参照],[16.8.1 参照]
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
同時に投与すると、紅斑、ヒスタミン様潮紅、アナフィラキシー反応等の副作用が発現することがある。 |
全身麻酔薬には、アナフィラキシー作用、ヒスタミン遊離作用を有するものがあり、本剤にもヒスタミン遊離作用がある。しかし、相互作用の機序は不明である。 |
|
|
腎障害、聴覚障害が発現、悪化するおそれがあるので、併用は避けること。やむを得ず併用する場合は、慎重に投与すること。 |
機序:両剤共に腎毒性、聴器毒性を有するが、相互作用の機序は不明である。 |
|
腎障害が発現、悪化するおそれがあるので、併用は避けること。やむを得ず併用する場合は、慎重に投与すること。 |
機序:両剤共に腎毒性を有するが、相互作用の機序は不明である。 |
11. 副作用
11.1 重大な副作用
-
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
ショック、アナフィラキシー(呼吸困難、全身潮紅、浮腫等)を起こすことがある。[8.2 参照]
-
11.1.2 急性腎障害、間質性腎炎(いずれも頻度不明)
急性腎障害、間質性腎炎等の重篤な腎障害があらわれることがある。[8.4 参照]
- 11.1.3 汎血球減少、無顆粒球症、血小板減少(いずれも頻度不明)
- 11.1.4 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、剥脱性皮膚炎(いずれも頻度不明)
-
11.1.5 薬剤性過敏症症候群(頻度不明)
初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがある。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること2) 。
- 11.1.6 第8脳神経障害(頻度不明)
-
11.1.7 偽膜性大腸炎(頻度不明)
偽膜性大腸炎等の血便を伴う重篤な大腸炎があらわれることがあるので、腹痛、頻回の下痢があらわれた場合には、直ちに投与を中止するなど適切な処置を行うこと。
-
11.1.8 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、Al-P等の上昇、黄疸があらわれることがある。[8.6 参照]
11.2 その他の副作用
2%以上 |
2%未満 |
頻度不明 |
|
|---|---|---|---|
過敏症 |
発疹 |
発赤、顔面潮紅 |
そう痒、蕁麻疹、線状IgA水疱症 |
肝臓 |
AST上昇、ALT上昇、ビリルビン上昇 |
Al-P上昇、LDH上昇 |
γ-GTP上昇、LAP上昇 |
腎臓 |
BUN上昇 |
クレアチニン上昇 |
|
血液 |
白血球減少、血小板減少、好酸球増多 |
貧血 |
|
消化器 |
下痢 |
嘔気、嘔吐、腹痛 |
|
その他 |
発熱、静脈炎、血管痛 |
皮膚血管炎、悪寒、注射部疼痛 |