薬効分類名セロイドリポフスチン症2型治療剤
一般的名称セルリポナーゼ アルファ(遺伝子組換え)
ブリニューラ脳室内注射液150mg
ぶりにゅーらのうしつないちゅうしゃえき
Brineura Intracerebroventricular Injectable Solution 150mg
製造販売業者/BioMarin Pharmaceutical Japan株式会社、製造業者/BioMarin International Limited, Ireland
第5版
警告禁忌合併症・既往歴等のある患者妊婦授乳婦小児等
重大な副作用
頻度
副作用
頻度不明
その他の副作用
部位
頻度
副作用
1. 警告
- 1.1 アナフィラキシーが発現することがあるので、緊急時に十分な対応のできる準備をした上で投与を開始し、投与終了後も十分な観察を行うこと。[11.1.1 参照]
4. 効能・効果
セロイドリポフスチン症2型
6. 用法・用量
通常、セルリポナーゼ アルファ(遺伝子組換え)として、300mgを2週間に1回、脳室内投与する。なお、患者の状態、年齢に応じて適宜減量する。
7. 用法・用量に関連する注意
-
7.1 2歳未満の患者では、下表を参考に減量すること。[9.7 参照]
年齢
1回投与量
出生~生後6カ月未満
100mg
生後6カ月~1歳未満
150mg
1歳~2歳未満
初めの4回目までの投与量:200mg
5回目以降の投与量:300mg - 7.2 通常、注入ポンプを用いて2.5mL/時間の速度で投与するが、患者の状態に応じて、投与速度を下げて投与すること。
- 7.3 本剤は、脳室内投与の知識、経験がある医師が投与すること。
- 7.4 本剤の投与によりアナフィラキシーを含む過敏症反応が発現することがある。症状を軽減させるため、患者の状態を考慮した上で、抗ヒスタミン剤を単独又は解熱鎮痛剤との併用で本剤投与開始30~60分前に前投与すること。[11.1.1 参照]
- 7.5 本剤投与中に、頭痛、悪心、嘔吐、精神状態の変化等の症状により投与中の頭蓋内圧が上昇していると判断される場合、投与の中断、投与速度を下げる等の適切な処置を行うこと。
- 7.6 本剤投与後、脳室アクセスデバイスを含む投与機器内の残存薬液を投与して脳室アクセスデバイスの開存性を維持するため、必要量を計算したフラッシュ溶液で脳室アクセスデバイスを含む投与機器内をフラッシュすること。[14.4.3 参照]
8. 重要な基本的注意
-
8.1 医療機器関連の合併症として、髄膜炎を含む感染症、脳室アクセスデバイスからの漏出、医療機器の不具合等がおこることがあるので、以下の点に注意すること。
- 脳室アクセスデバイスからの漏出、医療機器の不具合等に対する適切な対応をとれるよう体制を整えておくこと。
- 感染リスクを低減するため、本剤の投与は無菌的操作により行うこと。
- 本剤の投与前に、毎回、脳室アクセスデバイスからの漏出、医療機器の不具合又は感染症の兆候の有無を確認するために、植込み部分の皮膚に異常がないか確認すること。なお、脳室アクセスデバイスからの漏出又医療機器の不具合の一般的な徴候として、頭皮の腫脹・紅斑、体液溢出、頭皮周囲や脳室アクセスデバイス上部の膨隆などがある。[2.2 参照],[14.2 参照]
- 本剤の投与前に、毎回、脳脊髄液を吸引し、脳室アクセスデバイスの開存性を確認すること。医療機器関連感染症は無症候性の場合があるため、定期的に脳脊髄液検体を検査すること。[2.2 参照],[14.4.2 参照]
- 医療機器関連合併症が認められた場合は本剤の投与は行わず、適切な処置を行うこと。医療機器の不具合等については、各医療機器の添付文書も参照すること。[2.2 参照]
- 髄膜炎が認められた場合は、抗生物質の投与、脳室アクセスデバイスの交換を検討すること。
- 脳室アクセスデバイスは長期間の使用によって材質劣化を起こすことが繰返し穿刺試験や臨床試験で確認されているため、本剤投与が4年間継続される前に脳室アクセスデバイスの交換を検討すること。
- 8.2 アナフィラキシーを含む過敏症反応が発現する可能性があるため、以下の点に注意すること。[11.1.1 参照]
- 8.3 本剤との関連性は明らかではないが、本剤投与時に徐脈、低血圧等が認められているため、以下の点に注意すること。[9.1.1 参照]
14. 適用上の注意
14.1 全般的な注意
本剤の詳細な使用方法は、投与ガイドを確認すること。
14.2 薬剤適用に関する注意
14.3 薬剤調製時の注意
14.4 薬剤投与時の注意
-
14.4.1 全般的な注意
- (1) 本剤及びフラッシュ溶液の投与は無菌的操作により行うこと。
-
(2) 本剤及びフラッシュ溶液は外科的に留置した脳室アクセスデバイス(リザーバー及びカテーテル)を含む脳室内投与システムを用いて投与する(図1)。脳室アクセスデバイス、注入ポンプ及びチューブ等の医療機器の添付文書、取扱説明書等を熟読し、これらの注意に適切に対応すること。
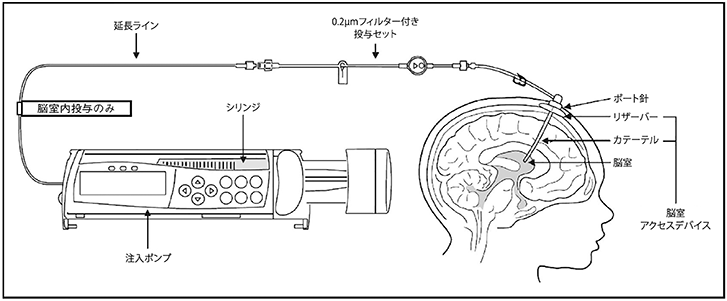
図1 脳室内投与システムの例 - (3) 脳室内投与システムに用いる医療機器は、本剤及びフラッシュ溶液との適合性の確認されたものを用いること。
- (4) 誤投与防止のために、本剤投与用シリンジ、フラッシュ溶液投与用シリンジ及び投与セット又は延長ラインに、「ブリニューラ脳室内注射液150mg」、「フラッシュ溶液」及び「脳室内投与のみ」と記載されたラベルをそれぞれ貼付すること。
- (5) 本剤及びフラッシュ溶液は希釈や他の医薬品との混合はしないこと。
- (6) 本剤及びフラッシュ溶液は注入ポンプで投与し、ボーラス又は手動で投与しないこと。
- (7) 注入ポンプは、閉塞を検知するために、アラーム音(閉塞アラーム)を設定して用いること。
- (8) 本剤を投与中は定期的に、漏出又は投与不具合の徴候がないか、脳室内投与システムを確認すること。
-
14.4.2 本剤の投与
- (1) シリンジに本剤を必要量(1回投与量が300mgの場合10mL、200mgの場合6.7mL、150mgの場合5mL、100mgの場合3.3mL)抜き取る。
- (2) 本剤を充填したシリンジを0.2μmフィルター付き投与セットに接続し、本剤で充填する。また、投与セットは延長ラインと接続することも可能である。
- (3) ポート針を脳室アクセスデバイスに挿入する。
- (4) 空のシリンジ(3mL以下)をポート針に接続し、脳脊髄液を0.5~1mL吸引し、脳室アクセスデバイスの開存性の確認及び感染症に関する検査を行うこと。なお、吸引した脳脊髄液を脳室アクセスデバイスに戻さないこと。[8.1 参照]
- (5) 投与セットをポート針に取り付ける。
- (6) 本剤を充填したシリンジを注入ポンプに設置し、本剤を2.5mL/時間の速度で投与する。
- 14.4.3 フラッシュ溶液の投与
1. 警告
- 1.1 アナフィラキシーが発現することがあるので、緊急時に十分な対応のできる準備をした上で投与を開始し、投与終了後も十分な観察を行うこと。[11.1.1 参照]
4. 効能・効果
セロイドリポフスチン症2型
6. 用法・用量
通常、セルリポナーゼ アルファ(遺伝子組換え)として、300mgを2週間に1回、脳室内投与する。なお、患者の状態、年齢に応じて適宜減量する。
7. 用法・用量に関連する注意
-
7.1 2歳未満の患者では、下表を参考に減量すること。[9.7 参照]
年齢
1回投与量
出生~生後6カ月未満
100mg
生後6カ月~1歳未満
150mg
1歳~2歳未満
初めの4回目までの投与量:200mg
5回目以降の投与量:300mg - 7.2 通常、注入ポンプを用いて2.5mL/時間の速度で投与するが、患者の状態に応じて、投与速度を下げて投与すること。
- 7.3 本剤は、脳室内投与の知識、経験がある医師が投与すること。
- 7.4 本剤の投与によりアナフィラキシーを含む過敏症反応が発現することがある。症状を軽減させるため、患者の状態を考慮した上で、抗ヒスタミン剤を単独又は解熱鎮痛剤との併用で本剤投与開始30~60分前に前投与すること。[11.1.1 参照]
- 7.5 本剤投与中に、頭痛、悪心、嘔吐、精神状態の変化等の症状により投与中の頭蓋内圧が上昇していると判断される場合、投与の中断、投与速度を下げる等の適切な処置を行うこと。
- 7.6 本剤投与後、脳室アクセスデバイスを含む投与機器内の残存薬液を投与して脳室アクセスデバイスの開存性を維持するため、必要量を計算したフラッシュ溶液で脳室アクセスデバイスを含む投与機器内をフラッシュすること。[14.4.3 参照]
8. 重要な基本的注意
-
8.1 医療機器関連の合併症として、髄膜炎を含む感染症、脳室アクセスデバイスからの漏出、医療機器の不具合等がおこることがあるので、以下の点に注意すること。
- 脳室アクセスデバイスからの漏出、医療機器の不具合等に対する適切な対応をとれるよう体制を整えておくこと。
- 感染リスクを低減するため、本剤の投与は無菌的操作により行うこと。
- 本剤の投与前に、毎回、脳室アクセスデバイスからの漏出、医療機器の不具合又は感染症の兆候の有無を確認するために、植込み部分の皮膚に異常がないか確認すること。なお、脳室アクセスデバイスからの漏出又医療機器の不具合の一般的な徴候として、頭皮の腫脹・紅斑、体液溢出、頭皮周囲や脳室アクセスデバイス上部の膨隆などがある。[2.2 参照],[14.2 参照]
- 本剤の投与前に、毎回、脳脊髄液を吸引し、脳室アクセスデバイスの開存性を確認すること。医療機器関連感染症は無症候性の場合があるため、定期的に脳脊髄液検体を検査すること。[2.2 参照],[14.4.2 参照]
- 医療機器関連合併症が認められた場合は本剤の投与は行わず、適切な処置を行うこと。医療機器の不具合等については、各医療機器の添付文書も参照すること。[2.2 参照]
- 髄膜炎が認められた場合は、抗生物質の投与、脳室アクセスデバイスの交換を検討すること。
- 脳室アクセスデバイスは長期間の使用によって材質劣化を起こすことが繰返し穿刺試験や臨床試験で確認されているため、本剤投与が4年間継続される前に脳室アクセスデバイスの交換を検討すること。
- 8.2 アナフィラキシーを含む過敏症反応が発現する可能性があるため、以下の点に注意すること。[11.1.1 参照]
- 8.3 本剤との関連性は明らかではないが、本剤投与時に徐脈、低血圧等が認められているため、以下の点に注意すること。[9.1.1 参照]
14. 適用上の注意
14.1 全般的な注意
本剤の詳細な使用方法は、投与ガイドを確認すること。
14.2 薬剤適用に関する注意
14.3 薬剤調製時の注意
14.4 薬剤投与時の注意
-
14.4.1 全般的な注意
- (1) 本剤及びフラッシュ溶液の投与は無菌的操作により行うこと。
-
(2) 本剤及びフラッシュ溶液は外科的に留置した脳室アクセスデバイス(リザーバー及びカテーテル)を含む脳室内投与システムを用いて投与する(図1)。脳室アクセスデバイス、注入ポンプ及びチューブ等の医療機器の添付文書、取扱説明書等を熟読し、これらの注意に適切に対応すること。

図1 脳室内投与システムの例 - (3) 脳室内投与システムに用いる医療機器は、本剤及びフラッシュ溶液との適合性の確認されたものを用いること。
- (4) 誤投与防止のために、本剤投与用シリンジ、フラッシュ溶液投与用シリンジ及び投与セット又は延長ラインに、「ブリニューラ脳室内注射液150mg」、「フラッシュ溶液」及び「脳室内投与のみ」と記載されたラベルをそれぞれ貼付すること。
- (5) 本剤及びフラッシュ溶液は希釈や他の医薬品との混合はしないこと。
- (6) 本剤及びフラッシュ溶液は注入ポンプで投与し、ボーラス又は手動で投与しないこと。
- (7) 注入ポンプは、閉塞を検知するために、アラーム音(閉塞アラーム)を設定して用いること。
- (8) 本剤を投与中は定期的に、漏出又は投与不具合の徴候がないか、脳室内投与システムを確認すること。
-
14.4.2 本剤の投与
- (1) シリンジに本剤を必要量(1回投与量が300mgの場合10mL、200mgの場合6.7mL、150mgの場合5mL、100mgの場合3.3mL)抜き取る。
- (2) 本剤を充填したシリンジを0.2μmフィルター付き投与セットに接続し、本剤で充填する。また、投与セットは延長ラインと接続することも可能である。
- (3) ポート針を脳室アクセスデバイスに挿入する。
- (4) 空のシリンジ(3mL以下)をポート針に接続し、脳脊髄液を0.5~1mL吸引し、脳室アクセスデバイスの開存性の確認及び感染症に関する検査を行うこと。なお、吸引した脳脊髄液を脳室アクセスデバイスに戻さないこと。[8.1 参照]
- (5) 投与セットをポート針に取り付ける。
- (6) 本剤を充填したシリンジを注入ポンプに設置し、本剤を2.5mL/時間の速度で投与する。
- 14.4.3 フラッシュ溶液の投与
その他詳細情報
日本標準商品分類番号
873959
ブランドコード
3959422A1028
承認番号
30100AMX00236000
販売開始年月
2020-01
貯法
-20℃以下で保存
有効期間
2年
規制区分
2, 12, 13