薬効分類名潰瘍性大腸炎治療剤
一般的名称メサラジン注腸1%製剤
メサラジン注腸1g「JG」
めさらじんちゅうちょう1g「JG」
Mesalazine Enema
製造販売元/日本ジェネリック株式会社
第4版
禁忌相互作用合併症・既往歴等のある患者腎機能障害患者肝機能障害患者妊婦授乳婦小児等高齢者
重大な副作用
頻度
副作用
その他の副作用
部位
頻度
副作用
併用注意
薬剤名等
- 利尿剤
- ステロイド剤
臨床症状・措置方法
臨床検査値(尿量、尿中ナトリウム、カリウム及び塩素イオン)の変動に注意する。
機序・危険因子
動物実験(ラット)で、メサラジンの大量投与(300mg/kg)により、尿量及びこれらイオンの排泄増加がみられる。
薬剤名等
- アザチオプリン
- メルカプトプリン
臨床症状・措置方法
骨髄抑制があらわれるおそれがある。
機序・危険因子
本剤は、チオプリンメチルトランスフェラーゼ活性を抑制するなど、これらの薬剤の代謝を阻害するとの報告がある,。
2. 禁忌(次の患者には投与しないこと)
- 2.1 重篤な腎障害のある患者[9.2.1 参照]
- 2.2 重篤な肝障害のある患者[9.3.1 参照]
- 2.3 本剤の成分に対し過敏症の既往歴のある患者[8.1 参照]
- 2.4 サリチル酸エステル類又はサリチル酸塩類に対する過敏症の既往歴のある患者[交叉アレルギーを発現するおそれがある。]
4. 効能又は効果
潰瘍性大腸炎(重症を除く)
5. 効能又は効果に関連する注意
脾彎曲部より口側の炎症には効果が期待できない。[16.8 参照]
6. 用法及び用量
通常、成人には1日1個(メサラジンとして1g)を、直腸内注入する。なお、年齢、症状により適宜減量する。
7. 用法及び用量に関連する注意
- 7.1 本剤をメサラジン経口剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、特に肝又は腎機能の低下している患者並びに高齢者等への投与に際しては十分に注意すること。併用時に異常が認められた場合には、減量又は中止する等の適切な処置を行うこと。[9.2.2 参照],[9.3.2 参照],[9.8 参照]
8. 重要な基本的注意
- 8.2 メサラジン錠において、間質性腎炎10) ,11) ,12) が報告されているため、投与中はクレアチニン等の腎機能をモニターする等、患者の状態を十分に観察すること。 [9.2.2 参照],[11.1.3 参照]
- 8.4 メサラジン錠において、肝炎21) ,22) ,23) 、肝機能障害、黄疸が報告されているため、投与中はAST、ALT等の肝機能をモニターする等、患者の状態を十分に観察すること。[9.3.2 参照],[11.1.5 参照]
- 8.5 膵炎24) ,25) があらわれることがあるので、投与期間中は血清アミラーゼの検査等を行うこと。[11.1.6 参照]
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
- 11.1.4 再生不良性貧血、汎血球減少、無顆粒球症、血小板減少症(いずれも頻度不明) [8.3 参照]
- 11.1.5 肝炎、肝機能障害、黄疸(いずれも頻度不明)肝炎、AST、ALT、γ-GTPの上昇等を伴う肝機能障害、黄疸があらわれることがある。[8.4 参照]
- 11.1.6 膵炎(頻度不明) [8.5 参照]
- 11.1.7 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN) (頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)
- 11.1.8 薬剤性過敏症症候群(頻度不明)初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがある。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること。
- 11.1.9 **抗好中球細胞質抗体(ANCA)関連血管炎(頻度不明)発熱、倦怠感、関節痛、筋痛等の全身症状や、皮膚(紅斑、紫斑)、肺(血痰)、腎臓(血尿、蛋白尿)等の臓器症状があらわれることがある。
11.2 その他の副作用
副作用頻度は、国内のペンタサ錠250mg・500mgの臨床成績及び市販後調査結果、又は外国における市販後調査結果(経口剤、注腸剤、坐剤を区別していない)
14. 適用上の注意
14.1 薬剤交付時の注意
14.2 薬剤投与後の注意
メサラジン又はその代謝物を含む尿は、次亜塩素酸塩を含有する漂白剤と接触することにより赤褐色に変色することがある。
2. 禁忌(次の患者には投与しないこと)
- 2.1 重篤な腎障害のある患者[9.2.1 参照]
- 2.2 重篤な肝障害のある患者[9.3.1 参照]
- 2.3 本剤の成分に対し過敏症の既往歴のある患者[8.1 参照]
- 2.4 サリチル酸エステル類又はサリチル酸塩類に対する過敏症の既往歴のある患者[交叉アレルギーを発現するおそれがある。]
4. 効能又は効果
潰瘍性大腸炎(重症を除く)
5. 効能又は効果に関連する注意
脾彎曲部より口側の炎症には効果が期待できない。[16.8 参照]
6. 用法及び用量
通常、成人には1日1個(メサラジンとして1g)を、直腸内注入する。なお、年齢、症状により適宜減量する。
7. 用法及び用量に関連する注意
- 7.1 本剤をメサラジン経口剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、特に肝又は腎機能の低下している患者並びに高齢者等への投与に際しては十分に注意すること。併用時に異常が認められた場合には、減量又は中止する等の適切な処置を行うこと。[9.2.2 参照],[9.3.2 参照],[9.8 参照]
8. 重要な基本的注意
- 8.2 メサラジン錠において、間質性腎炎10) ,11) ,12) が報告されているため、投与中はクレアチニン等の腎機能をモニターする等、患者の状態を十分に観察すること。 [9.2.2 参照],[11.1.3 参照]
- 8.4 メサラジン錠において、肝炎21) ,22) ,23) 、肝機能障害、黄疸が報告されているため、投与中はAST、ALT等の肝機能をモニターする等、患者の状態を十分に観察すること。[9.3.2 参照],[11.1.5 参照]
- 8.5 膵炎24) ,25) があらわれることがあるので、投与期間中は血清アミラーゼの検査等を行うこと。[11.1.6 参照]
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
- 11.1.4 再生不良性貧血、汎血球減少、無顆粒球症、血小板減少症(いずれも頻度不明) [8.3 参照]
- 11.1.5 肝炎、肝機能障害、黄疸(いずれも頻度不明)肝炎、AST、ALT、γ-GTPの上昇等を伴う肝機能障害、黄疸があらわれることがある。[8.4 参照]
- 11.1.6 膵炎(頻度不明) [8.5 参照]
- 11.1.7 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN) (頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)
- 11.1.8 薬剤性過敏症症候群(頻度不明)初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがある。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること。
- 11.1.9 **抗好中球細胞質抗体(ANCA)関連血管炎(頻度不明)発熱、倦怠感、関節痛、筋痛等の全身症状や、皮膚(紅斑、紫斑)、肺(血痰)、腎臓(血尿、蛋白尿)等の臓器症状があらわれることがある。
11.2 その他の副作用
副作用頻度は、国内のペンタサ錠250mg・500mgの臨床成績及び市販後調査結果、又は外国における市販後調査結果(経口剤、注腸剤、坐剤を区別していない)
14. 適用上の注意
14.1 薬剤交付時の注意
14.2 薬剤投与後の注意
メサラジン又はその代謝物を含む尿は、次亜塩素酸塩を含有する漂白剤と接触することにより赤褐色に変色することがある。
その他詳細情報
日本標準商品分類番号
872399
ブランドコード
2399715X1031
承認番号
22400AMX00550000
販売開始年月
2012-06
貯法
室温保存
有効期間
3年
規制区分
12
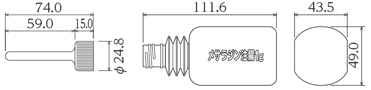 ノズル延長用カテーテル ストッパー
ノズル延長用カテーテル ストッパー