薬効分類名
一般的名称硝酸イソソルビド
ニトロール点滴静注50mgバッグ、ニトロール点滴静注100mgバッグ
にとろーるてんてきじょうちゅうばっぐ、にとろーるてんてきじょうちゅうばっぐ
Nitorol for Intravenous Drip Infusion, Nitorol for Intravenous Drip Infusion
製造販売元/エーザイ株式会社
重大な副作用
その他の副作用
併用注意
利尿剤
血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。
血圧低下作用を増強させる。
血管拡張剤
硝酸・亜硝酸エステル系薬剤
血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。
血管拡張作用が増強される。
2. 禁忌(次の患者には投与しないこと)
- 2.1 重篤な低血圧又は心原性ショックのある患者[血管拡張作用によりさらに血圧を低下させ、症状を悪化させるおそれがある。][9.1.1 参照]
- 2.2 Eisenmenger症候群又は原発性肺高血圧症の患者[血圧低下によりショックを起こすことがある。]
- 2.3 右室梗塞の患者[血圧低下によりショックを起こすことがある。]
- 2.4 脱水症状のある患者[血圧低下によりショックを起こすことがある。]
- 2.5 神経循環無力症の患者[本剤の効果がなく、本剤投与により血圧低下等があらわれることがある。]
- 2.6 閉塞隅角緑内障の患者[眼圧を上昇させるおそれがある。]
- 2.7 硝酸・亜硝酸エステル系薬剤に対し過敏症の既往歴のある患者
- 2.8 頭部外傷又は脳出血のある患者[頭蓋内圧を上昇させるおそれがある。]
- 2.9 ホスホジエステラーゼ5阻害作用を有する薬剤(シルデナフィルクエン酸塩、バルデナフィル塩酸塩水和物、タダラフィル)又はグアニル酸シクラーゼ刺激作用を有する薬剤(リオシグアト)を投与中の患者[10.1 参照]
8. 重要な基本的注意
- 8.1 本剤投与中は、頻回の血圧測定と血行動態のモニターを行うこと。また、投与量の調節は患者の血行動態、症状をみて徐々に行うこと。[11.1.1 参照]
- 8.2 投与中に血圧低下等の異常が観察された場合には、減量又は投与を中止すること。また、必要に応じて昇圧剤投与等の適切な処置を行うこと。[11.1.1 参照]
- 8.3 血圧低下の可能性のある患者や心拍出量が低下している患者に投与する場合には、カテコールアミン系薬剤等と併用することが望ましい。
- 8.4 投与中に左心不全状態が改善した場合は、患者の様子をみて投与を中止すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 低血圧の患者(重篤な低血圧のある患者を除く)
さらに血圧を低下させるおそれがある。[2.1 参照]
-
9.1.2 左室充満圧の低い患者
血圧低下及び心拍出量低下のおそれがある。
-
9.1.3 遺伝性果糖不耐症の患者
本剤の添加剤D-ソルビトールが体内で代謝されて生成した果糖が正常に代謝されず、低血糖、肝不全、腎不全等が誘発されるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
本剤は、主として肝臓で代謝されるが、一般に肝機能が低下していることが多いため、高い血中濃度が持続するおそれがある。
10. 相互作用
10.1 併用禁忌(併用しないこと)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
ホスホジエステラーゼ5阻害作用を有する薬剤 |
併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 |
本剤はcGMPの産生を促進し、一方、ホスホジエステラーゼ5阻害作用を有する薬剤はcGMPの分解を抑制することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 |
本剤とグアニル酸シクラーゼ刺激作用を有する薬剤は、ともにcGMPの産生を促進することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
利尿剤 |
血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 |
血圧低下作用を増強させる。 |
血管拡張剤 |
血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 |
血管拡張作用が増強される。 |
14. 適用上の注意
14.1 薬剤投与時の注意
- 14.1.1 注射針はゴム栓の○印にまっすぐ刺すこと。斜めに刺すと注射針が容器頸部を貫通し、液漏れの原因となることがある。
- 14.1.2 原則として連結管(U字管)を用いたタンデム方式による投与はできない。
- 14.1.3 容器の液目盛りはおよその目安として使用すること。
-
14.1.4 輸液セットへの吸着
硝酸イソソルビドは、一般に使用されているポリ塩化ビニル製の輸液容器及び輸液セットに吸着するが、ガラス製、ポリエチレン製の容器、器具には吸着しない。硝酸イソソルビドのポリ塩化ビニル製輸液セットに対する吸着率は、図に示す通りで点滴速度に影響され、ポリ塩化ビニル管100cmでは点滴速度60mL/時間(1mL/分)以上であれば、投与量の80%以上が静脈内に注入される。また、硝酸イソソルビドの吸着率は配合濃度に影響されないが、輸液セットが長い程高くなるので注意すること。
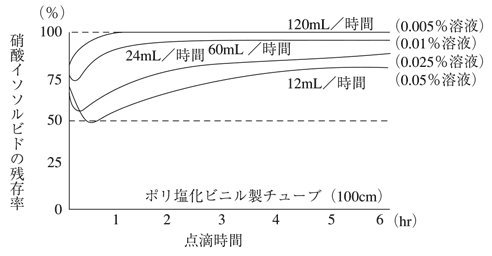
点滴速度による影響
2. 禁忌(次の患者には投与しないこと)
- 2.1 重篤な低血圧又は心原性ショックのある患者[血管拡張作用によりさらに血圧を低下させ、症状を悪化させるおそれがある。][9.1.1 参照]
- 2.2 Eisenmenger症候群又は原発性肺高血圧症の患者[血圧低下によりショックを起こすことがある。]
- 2.3 右室梗塞の患者[血圧低下によりショックを起こすことがある。]
- 2.4 脱水症状のある患者[血圧低下によりショックを起こすことがある。]
- 2.5 神経循環無力症の患者[本剤の効果がなく、本剤投与により血圧低下等があらわれることがある。]
- 2.6 閉塞隅角緑内障の患者[眼圧を上昇させるおそれがある。]
- 2.7 硝酸・亜硝酸エステル系薬剤に対し過敏症の既往歴のある患者
- 2.8 頭部外傷又は脳出血のある患者[頭蓋内圧を上昇させるおそれがある。]
- 2.9 ホスホジエステラーゼ5阻害作用を有する薬剤(シルデナフィルクエン酸塩、バルデナフィル塩酸塩水和物、タダラフィル)又はグアニル酸シクラーゼ刺激作用を有する薬剤(リオシグアト)を投与中の患者[10.1 参照]
8. 重要な基本的注意
- 8.1 本剤投与中は、頻回の血圧測定と血行動態のモニターを行うこと。また、投与量の調節は患者の血行動態、症状をみて徐々に行うこと。[11.1.1 参照]
- 8.2 投与中に血圧低下等の異常が観察された場合には、減量又は投与を中止すること。また、必要に応じて昇圧剤投与等の適切な処置を行うこと。[11.1.1 参照]
- 8.3 血圧低下の可能性のある患者や心拍出量が低下している患者に投与する場合には、カテコールアミン系薬剤等と併用することが望ましい。
- 8.4 投与中に左心不全状態が改善した場合は、患者の様子をみて投与を中止すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 低血圧の患者(重篤な低血圧のある患者を除く)
さらに血圧を低下させるおそれがある。[2.1 参照]
-
9.1.2 左室充満圧の低い患者
血圧低下及び心拍出量低下のおそれがある。
-
9.1.3 遺伝性果糖不耐症の患者
本剤の添加剤D-ソルビトールが体内で代謝されて生成した果糖が正常に代謝されず、低血糖、肝不全、腎不全等が誘発されるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
本剤は、主として肝臓で代謝されるが、一般に肝機能が低下していることが多いため、高い血中濃度が持続するおそれがある。
10. 相互作用
10.1 併用禁忌(併用しないこと)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
ホスホジエステラーゼ5阻害作用を有する薬剤 |
併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 |
本剤はcGMPの産生を促進し、一方、ホスホジエステラーゼ5阻害作用を有する薬剤はcGMPの分解を抑制することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 |
本剤とグアニル酸シクラーゼ刺激作用を有する薬剤は、ともにcGMPの産生を促進することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
利尿剤 |
血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 |
血圧低下作用を増強させる。 |
血管拡張剤 |
血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 |
血管拡張作用が増強される。 |
14. 適用上の注意
14.1 薬剤投与時の注意
- 14.1.1 注射針はゴム栓の○印にまっすぐ刺すこと。斜めに刺すと注射針が容器頸部を貫通し、液漏れの原因となることがある。
- 14.1.2 原則として連結管(U字管)を用いたタンデム方式による投与はできない。
- 14.1.3 容器の液目盛りはおよその目安として使用すること。
-
14.1.4 輸液セットへの吸着
硝酸イソソルビドは、一般に使用されているポリ塩化ビニル製の輸液容器及び輸液セットに吸着するが、ガラス製、ポリエチレン製の容器、器具には吸着しない。硝酸イソソルビドのポリ塩化ビニル製輸液セットに対する吸着率は、図に示す通りで点滴速度に影響され、ポリ塩化ビニル管100cmでは点滴速度60mL/時間(1mL/分)以上であれば、投与量の80%以上が静脈内に注入される。また、硝酸イソソルビドの吸着率は配合濃度に影響されないが、輸液セットが長い程高くなるので注意すること。

点滴速度による影響