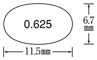薬効分類名結合型エストロゲン製剤
一般的名称結合型エストロゲン
プレマリン錠0.625mg
ぷれまりんじょう0.625mg
PREMARIN TABLETS 0.625mg
製造販売元/ファイザー株式会社
重大な副作用
その他の副作用
併用注意
イプリフラボン
エストロゲン作用(帯下、不正出血、経血量の変化等)が増強する可能性がある。
エストロゲンの作用を増加させる。
血糖降下剤
- グリベンクラミド
グリクラジド
アセトヘキサミド等
血糖降下剤の作用が減弱することがあるので、併用する場合には血糖値その他患者の状態を十分観察し、血糖降下剤の用量を調節するなど注意すること。
エストロゲンは耐糖能を低下させ、血糖を上昇させる作用が認められている。
副腎皮質ホルモン
- プレドニゾロン等
これらの薬剤の作用が増強するおそれがある。
エストロゲンはこれらの薬剤の代謝を抑制すると考えられる。
ソマトロピン(遺伝子組換え)
成長ホルモンの作用が抑制されることがある。成人成長ホルモン分泌不全症(重症に限る)の患者に併用する場合は、ソマトロピンの増量を検討すること。
エストロゲンがIGF-I産生を抑制するため。
ソムアトロゴン( 遺伝子組換え)
成長ホルモンの成長促進作用が抑制されることがある。
エストロゲンがIGF-I産生を抑制するため。
2. 禁忌(次の患者には投与しないこと)
- 2.1 エストロゲン依存性腫瘍(例えば乳癌、子宮内膜癌)及びその疑いのある患者[腫瘍の悪化あるいは顕性化を促すことがある。][8.2 参照]
- 2.2 乳癌の既往歴のある患者[8.2 参照]
- 2.3 血栓性静脈炎や肺塞栓症のある患者、又はその既往歴のある患者[エストロゲンは凝固因子を増加させ、血栓形成傾向を促進するとの報告がある。][11.1.1 参照]
- 2.4 動脈性の血栓塞栓疾患(例えば、冠動脈性心疾患、脳卒中)又はその既往歴のある患者[11.1.1 参照],[15.1.3 参照],[15.1.4 参照]
- 2.5 本剤の成分に対し過敏症の既往歴のある患者
- 2.6 妊婦又は妊娠している可能性のある女性[9.5.1 参照]
- 2.7 重篤な肝障害のある患者[9.3.1 参照]
- 2.8 診断の確定していない異常性器出血のある患者[出血が子宮内膜癌による場合は、癌の悪化あるいは顕性化を促すことがある。][8.2 参照]
- 2.9 未治療の子宮内膜増殖症のある患者[子宮内膜増殖症は細胞異型を伴う場合がある。][8.2 参照]
4. 効能又は効果
卵巣欠落症状、卵巣機能不全症、更年期障害、腟炎(老人、小児および非特異性)、機能性子宮出血
6. 用法及び用量
結合型エストロゲンとして、通常成人1日0.625〜1.25mgを経口投与する。
機能性子宮出血又は腟炎に対しては、1日0.625〜3.75mgを経口投与する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
- 8.1 **外国において、卵胞ホルモン剤と黄体ホルモン剤を長期併用した女性では、乳癌になる危険性が対照群の女性と比較して高くなり、その危険性は併用期間が長期になるに従って高くなるとの報告があるので、本剤の投与にあたっては、患者に対し本剤のリスクとベネフィットについて十分な説明を行うとともに必要最小限の使用にとどめ、漫然と長期投与を行わないこと。[15.1.2 参照]
- 8.2 投与前に病歴、家族素因等の問診、乳房検診並びに婦人科検診(子宮を有する患者においては子宮内膜細胞診及び超音波検査による子宮内膜厚の測定を含む)を行い、投与開始後は定期的に乳房検診並びに婦人科検診を行うこと。[2.1 参照],[2.2 参照],[2.8 参照],[2.9 参照],[9.1.1 参照],[9.1.2 参照],[9.1.7 参照]
- 8.3 本剤の服用により、血栓症があらわれることがあるので、次のような症状・状態があらわれた場合は投与を中止すること。また、患者に対しては、次のような症状・状態が認められた場合には直ちに医師等に相談するよう、あらかじめ説明すること。[9.1.6 参照],[11.1.1 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 子宮内膜症のある患者
症状を悪化させるおそれがある。[8.2 参照]
-
9.1.2 子宮筋腫のある患者
子宮筋腫の発育を促進するおそれがある。[8.2 参照]
-
9.1.3 心疾患又はその既往歴のある患者
エストロゲンの過量投与では体液貯留を来し、心疾患を悪化させるおそれがある。
-
9.1.4 てんかんの患者
症状を悪化させることがある。
-
9.1.5 糖尿病患者
十分管理を行いながら使用すること。耐糖能を低下させるおそれがある。
-
9.1.6 手術前4週以内又は長期臥床状態の患者
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。血液凝固能が亢進し、血管系の副作用の危険性が高くなるおそれがある。[8.3 参照],[11.1.1 参照]
-
9.1.7 乳癌家族素因が強い患者、乳房結節のある患者、乳腺症の患者又は乳房レントゲン像に異常がみられた患者
症状を悪化させるおそれがある。[8.2 参照]
-
9.1.8 全身性エリテマトーデスの患者
症状を悪化させるおそれがある。
-
9.1.9 片頭痛の患者
症状を悪化させるおそれがある。前兆を伴う片頭痛は虚血性脳卒中を有するおそれがある。
-
9.1.10 思春期前の患者
卵胞ホルモン剤の投与により骨端の早期閉鎖を来すおそれがある。[9.7 参照]
9.3 肝機能障害患者
-
9.3.1 重篤な肝障害のある患者
投与しないこと。代謝能が低下しており肝臓への負担が増加するため、症状が増悪することがある。[2.7 参照]
-
9.3.2 肝障害のある患者(重篤な肝障害のある患者を除く)
肝障害を悪化させるおそれがある。
9.5 妊婦
- 9.5.1 妊婦又は妊娠している可能性のある女性には投与しないこと。[2.6 参照]
-
9.5.2 卵胞ホルモン剤を妊娠動物(マウス)に投与した場合、児の成長後腟上皮及び子宮内膜の癌性変性を示唆する結果が報告されている。
また、新生児に投与した場合、児の成長後腟上皮の癌性変性を認めたとの報告がある。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
イプリフラボン |
エストロゲン作用(帯下、不正出血、経血量の変化等)が増強する可能性がある。 |
エストロゲンの作用を増加させる。 |
血糖降下剤の作用が減弱することがあるので、併用する場合には血糖値その他患者の状態を十分観察し、血糖降下剤の用量を調節するなど注意すること。 |
エストロゲンは耐糖能を低下させ、血糖を上昇させる作用が認められている。 |
|
これらの薬剤の作用が増強するおそれがある。 |
エストロゲンはこれらの薬剤の代謝を抑制すると考えられる。 |
|
ソマトロピン(遺伝子組換え) |
成長ホルモンの作用が抑制されることがある。成人成長ホルモン分泌不全症(重症に限る)の患者に併用する場合は、ソマトロピンの増量を検討すること。 |
エストロゲンがIGF-I産生を抑制するため。 |
* ソムアトロゴン( 遺伝子組換え) |
成長ホルモンの成長促進作用が抑制されることがある。 |
エストロゲンがIGF-I産生を抑制するため。 |
11. 副作用
11.1 重大な副作用
-
11.1.1 血栓症(頻度不明)
血栓症あるいは血栓塞栓症(四肢、肺、心、脳、網膜等)があらわれることがあるので、観察を十分に行い、下肢の疼痛・浮腫、突然の呼吸困難、息切れ、胸痛、中枢神経症状(めまい、意識障害、四肢麻痺等)、急性視力障害等の初期症状があらわれた場合には投与を中止し、適切な処置を行うこと。[2.3 参照],[2.4 参照],[8.3 参照],[9.1.6 参照]
11.2 その他の副作用
頻度不明 |
|
|---|---|
電解質代謝注1) |
ナトリウムや体液の貯留(浮腫、体重増加等) |
生殖器 |
帯下増加、不正出血、経血量の変化 |
乳房 |
乳房痛、乳房緊満感 |
過敏症 |
発疹、蕁麻疹、血管性浮腫 |
消化器 |
腹痛、悪心・嘔吐、食欲不振、膵炎 |
皮膚 |
色素沈着、脱毛 |
精神神経系 |
頭痛、めまい |
肝臓 |
肝機能障害(AST、ALT、Al-P上昇等) |
呼吸器 |
呼吸困難 |
循環器 |
血圧低下 |
15. その他の注意
15.1 臨床使用に基づく情報
-
15.1.1 ホルモン補充療法(HRT)と子宮内膜癌の危険性
卵胞ホルモン剤を長期間(約1年以上)使用した閉経期以降の女性では、子宮内膜癌になる危険性が対照群の女性と比較して高く、この危険性は、使用期間に相関して上昇し(1〜5年間で2.8倍、10年以上で9.5倍)、黄体ホルモン剤の併用により抑えられる(対照群の女性と比較して0.8倍)との疫学調査の結果が報告されている1) 。
-
15.1.2 **HRTと乳癌の危険性
HRTと乳癌発生との因果関係については明らかではないが、次のような報告がある。
- (1) 米国における閉経後女性を対象とした無作為化臨床試験(Women's Health Initiative(WHI)試験)の結果、本剤と黄体ホルモンの配合剤投与群では、乳癌になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.24)との報告がある2) 。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、乳癌になる危険性がプラセボ投与群と比較して有意差はない(ハザード比:0.80)との報告がある3) ,4) 。[8.1 参照]
- (2) 英国における疫学調査(Million Women Study(MWS))の結果、卵胞ホルモン剤と黄体ホルモン剤を併用している女性では、乳癌になる危険性が対照群と比較して有意に高くなり(2.00倍)、この危険性は、併用期間が長期になるに従って高くなる(1年未満:1.45倍、1〜4年: 1.74倍、5〜9年:2.17倍、10年以上:2.31倍)との報告がある5) 。[8.1 参照]
- (3) 閉経後女性を対象とした大規模な疫学調査のメタアナリシスの結果、閉経期ホルモン補充療法(MHT)として卵胞ホルモン剤を単独投与又は卵胞ホルモン剤と黄体ホルモン剤を併用した女性は、乳癌になる危険性がMHTの期間とともに高くなり(調整リスク比[95%信頼区間]は1~4年間の卵胞ホルモン剤と黄体ホルモン剤併用:1.60[1.52–1.69]、卵胞ホルモン剤単独:1.17[1.10–1.26]、5~14年間の卵胞ホルモン剤と黄体ホルモン剤併用:2.08[2.02–2.15]、卵胞ホルモン剤単独:1.33[1.28–1.37])、MHT非使用者に対する調整リスク比はMHT過去使用者よりMHT現使用者の方が高かった。また、MHT過去使用者において、投与中止後も過去の投与期間に依存して乳癌になる危険性が10年以上持続する場合があるとの報告がある6) 。[8.1 参照]
-
15.1.3 HRTと冠動脈性心疾患の危険性
米国におけるWHI試験の結果、本剤と黄体ホルモンの配合剤投与群では、冠動脈性心疾患の危険性がプラセボ投与群と比較して高い傾向にあり、特に服用開始1年後では有意に高くなる(ハザード比:1.81)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、冠動脈性心疾患の危険性がプラセボ投与群と比較して有意差はない(ハザード比:0.91)との報告がある3) ,7) 。[2.4 参照]
-
15.1.4 HRTと脳卒中の危険性
米国におけるWHI試験の結果、本剤と黄体ホルモンの配合剤投与群では、脳卒中(主として脳梗塞)の危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.31)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、脳卒中(主として脳梗塞)の危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.37)との報告がある3) ,8) ,9) 。[2.4 参照]
-
15.1.5 HRTと認知症の危険性
米国における65歳以上の閉経後女性を対象とした無作為化臨床試験(WHI Memory Study(WHIMS))の結果、本剤と黄体ホルモンの配合剤投与群では、アルツハイマーを含む認知症の危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:2.05)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、アルツハイマーを含む認知症の危険性がプラセボ投与群と比較して有意ではないが、高い傾向がみられた(ハザード比:1.49)との報告がある10) ,11) 。
- 15.1.6 長期投与により肝腫瘍が発生したとの報告がある。
- 15.1.7 HRTと卵巣癌の危険性
-
15.1.8 HRTと胆嚢疾患の危険性
米国におけるWHI試験の結果、本剤と黄体ホルモンの配合剤投与群において、胆嚢疾患になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.59)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、胆嚢疾患になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.67)との報告がある16) 。
2. 禁忌(次の患者には投与しないこと)
- 2.1 エストロゲン依存性腫瘍(例えば乳癌、子宮内膜癌)及びその疑いのある患者[腫瘍の悪化あるいは顕性化を促すことがある。][8.2 参照]
- 2.2 乳癌の既往歴のある患者[8.2 参照]
- 2.3 血栓性静脈炎や肺塞栓症のある患者、又はその既往歴のある患者[エストロゲンは凝固因子を増加させ、血栓形成傾向を促進するとの報告がある。][11.1.1 参照]
- 2.4 動脈性の血栓塞栓疾患(例えば、冠動脈性心疾患、脳卒中)又はその既往歴のある患者[11.1.1 参照],[15.1.3 参照],[15.1.4 参照]
- 2.5 本剤の成分に対し過敏症の既往歴のある患者
- 2.6 妊婦又は妊娠している可能性のある女性[9.5.1 参照]
- 2.7 重篤な肝障害のある患者[9.3.1 参照]
- 2.8 診断の確定していない異常性器出血のある患者[出血が子宮内膜癌による場合は、癌の悪化あるいは顕性化を促すことがある。][8.2 参照]
- 2.9 未治療の子宮内膜増殖症のある患者[子宮内膜増殖症は細胞異型を伴う場合がある。][8.2 参照]
4. 効能又は効果
卵巣欠落症状、卵巣機能不全症、更年期障害、腟炎(老人、小児および非特異性)、機能性子宮出血
6. 用法及び用量
結合型エストロゲンとして、通常成人1日0.625〜1.25mgを経口投与する。
機能性子宮出血又は腟炎に対しては、1日0.625〜3.75mgを経口投与する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
- 8.1 **外国において、卵胞ホルモン剤と黄体ホルモン剤を長期併用した女性では、乳癌になる危険性が対照群の女性と比較して高くなり、その危険性は併用期間が長期になるに従って高くなるとの報告があるので、本剤の投与にあたっては、患者に対し本剤のリスクとベネフィットについて十分な説明を行うとともに必要最小限の使用にとどめ、漫然と長期投与を行わないこと。[15.1.2 参照]
- 8.2 投与前に病歴、家族素因等の問診、乳房検診並びに婦人科検診(子宮を有する患者においては子宮内膜細胞診及び超音波検査による子宮内膜厚の測定を含む)を行い、投与開始後は定期的に乳房検診並びに婦人科検診を行うこと。[2.1 参照],[2.2 参照],[2.8 参照],[2.9 参照],[9.1.1 参照],[9.1.2 参照],[9.1.7 参照]
- 8.3 本剤の服用により、血栓症があらわれることがあるので、次のような症状・状態があらわれた場合は投与を中止すること。また、患者に対しては、次のような症状・状態が認められた場合には直ちに医師等に相談するよう、あらかじめ説明すること。[9.1.6 参照],[11.1.1 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 子宮内膜症のある患者
症状を悪化させるおそれがある。[8.2 参照]
-
9.1.2 子宮筋腫のある患者
子宮筋腫の発育を促進するおそれがある。[8.2 参照]
-
9.1.3 心疾患又はその既往歴のある患者
エストロゲンの過量投与では体液貯留を来し、心疾患を悪化させるおそれがある。
-
9.1.4 てんかんの患者
症状を悪化させることがある。
-
9.1.5 糖尿病患者
十分管理を行いながら使用すること。耐糖能を低下させるおそれがある。
-
9.1.6 手術前4週以内又は長期臥床状態の患者
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。血液凝固能が亢進し、血管系の副作用の危険性が高くなるおそれがある。[8.3 参照],[11.1.1 参照]
-
9.1.7 乳癌家族素因が強い患者、乳房結節のある患者、乳腺症の患者又は乳房レントゲン像に異常がみられた患者
症状を悪化させるおそれがある。[8.2 参照]
-
9.1.8 全身性エリテマトーデスの患者
症状を悪化させるおそれがある。
-
9.1.9 片頭痛の患者
症状を悪化させるおそれがある。前兆を伴う片頭痛は虚血性脳卒中を有するおそれがある。
-
9.1.10 思春期前の患者
卵胞ホルモン剤の投与により骨端の早期閉鎖を来すおそれがある。[9.7 参照]
9.3 肝機能障害患者
-
9.3.1 重篤な肝障害のある患者
投与しないこと。代謝能が低下しており肝臓への負担が増加するため、症状が増悪することがある。[2.7 参照]
-
9.3.2 肝障害のある患者(重篤な肝障害のある患者を除く)
肝障害を悪化させるおそれがある。
9.5 妊婦
- 9.5.1 妊婦又は妊娠している可能性のある女性には投与しないこと。[2.6 参照]
-
9.5.2 卵胞ホルモン剤を妊娠動物(マウス)に投与した場合、児の成長後腟上皮及び子宮内膜の癌性変性を示唆する結果が報告されている。
また、新生児に投与した場合、児の成長後腟上皮の癌性変性を認めたとの報告がある。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
イプリフラボン |
エストロゲン作用(帯下、不正出血、経血量の変化等)が増強する可能性がある。 |
エストロゲンの作用を増加させる。 |
血糖降下剤の作用が減弱することがあるので、併用する場合には血糖値その他患者の状態を十分観察し、血糖降下剤の用量を調節するなど注意すること。 |
エストロゲンは耐糖能を低下させ、血糖を上昇させる作用が認められている。 |
|
これらの薬剤の作用が増強するおそれがある。 |
エストロゲンはこれらの薬剤の代謝を抑制すると考えられる。 |
|
ソマトロピン(遺伝子組換え) |
成長ホルモンの作用が抑制されることがある。成人成長ホルモン分泌不全症(重症に限る)の患者に併用する場合は、ソマトロピンの増量を検討すること。 |
エストロゲンがIGF-I産生を抑制するため。 |
* ソムアトロゴン( 遺伝子組換え) |
成長ホルモンの成長促進作用が抑制されることがある。 |
エストロゲンがIGF-I産生を抑制するため。 |
11. 副作用
11.1 重大な副作用
-
11.1.1 血栓症(頻度不明)
血栓症あるいは血栓塞栓症(四肢、肺、心、脳、網膜等)があらわれることがあるので、観察を十分に行い、下肢の疼痛・浮腫、突然の呼吸困難、息切れ、胸痛、中枢神経症状(めまい、意識障害、四肢麻痺等)、急性視力障害等の初期症状があらわれた場合には投与を中止し、適切な処置を行うこと。[2.3 参照],[2.4 参照],[8.3 参照],[9.1.6 参照]
11.2 その他の副作用
頻度不明 |
|
|---|---|
電解質代謝注1) |
ナトリウムや体液の貯留(浮腫、体重増加等) |
生殖器 |
帯下増加、不正出血、経血量の変化 |
乳房 |
乳房痛、乳房緊満感 |
過敏症 |
発疹、蕁麻疹、血管性浮腫 |
消化器 |
腹痛、悪心・嘔吐、食欲不振、膵炎 |
皮膚 |
色素沈着、脱毛 |
精神神経系 |
頭痛、めまい |
肝臓 |
肝機能障害(AST、ALT、Al-P上昇等) |
呼吸器 |
呼吸困難 |
循環器 |
血圧低下 |
15. その他の注意
15.1 臨床使用に基づく情報
-
15.1.1 ホルモン補充療法(HRT)と子宮内膜癌の危険性
卵胞ホルモン剤を長期間(約1年以上)使用した閉経期以降の女性では、子宮内膜癌になる危険性が対照群の女性と比較して高く、この危険性は、使用期間に相関して上昇し(1〜5年間で2.8倍、10年以上で9.5倍)、黄体ホルモン剤の併用により抑えられる(対照群の女性と比較して0.8倍)との疫学調査の結果が報告されている1) 。
-
15.1.2 **HRTと乳癌の危険性
HRTと乳癌発生との因果関係については明らかではないが、次のような報告がある。
- (1) 米国における閉経後女性を対象とした無作為化臨床試験(Women's Health Initiative(WHI)試験)の結果、本剤と黄体ホルモンの配合剤投与群では、乳癌になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.24)との報告がある2) 。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、乳癌になる危険性がプラセボ投与群と比較して有意差はない(ハザード比:0.80)との報告がある3) ,4) 。[8.1 参照]
- (2) 英国における疫学調査(Million Women Study(MWS))の結果、卵胞ホルモン剤と黄体ホルモン剤を併用している女性では、乳癌になる危険性が対照群と比較して有意に高くなり(2.00倍)、この危険性は、併用期間が長期になるに従って高くなる(1年未満:1.45倍、1〜4年: 1.74倍、5〜9年:2.17倍、10年以上:2.31倍)との報告がある5) 。[8.1 参照]
- (3) 閉経後女性を対象とした大規模な疫学調査のメタアナリシスの結果、閉経期ホルモン補充療法(MHT)として卵胞ホルモン剤を単独投与又は卵胞ホルモン剤と黄体ホルモン剤を併用した女性は、乳癌になる危険性がMHTの期間とともに高くなり(調整リスク比[95%信頼区間]は1~4年間の卵胞ホルモン剤と黄体ホルモン剤併用:1.60[1.52–1.69]、卵胞ホルモン剤単独:1.17[1.10–1.26]、5~14年間の卵胞ホルモン剤と黄体ホルモン剤併用:2.08[2.02–2.15]、卵胞ホルモン剤単独:1.33[1.28–1.37])、MHT非使用者に対する調整リスク比はMHT過去使用者よりMHT現使用者の方が高かった。また、MHT過去使用者において、投与中止後も過去の投与期間に依存して乳癌になる危険性が10年以上持続する場合があるとの報告がある6) 。[8.1 参照]
-
15.1.3 HRTと冠動脈性心疾患の危険性
米国におけるWHI試験の結果、本剤と黄体ホルモンの配合剤投与群では、冠動脈性心疾患の危険性がプラセボ投与群と比較して高い傾向にあり、特に服用開始1年後では有意に高くなる(ハザード比:1.81)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、冠動脈性心疾患の危険性がプラセボ投与群と比較して有意差はない(ハザード比:0.91)との報告がある3) ,7) 。[2.4 参照]
-
15.1.4 HRTと脳卒中の危険性
米国におけるWHI試験の結果、本剤と黄体ホルモンの配合剤投与群では、脳卒中(主として脳梗塞)の危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.31)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、脳卒中(主として脳梗塞)の危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.37)との報告がある3) ,8) ,9) 。[2.4 参照]
-
15.1.5 HRTと認知症の危険性
米国における65歳以上の閉経後女性を対象とした無作為化臨床試験(WHI Memory Study(WHIMS))の結果、本剤と黄体ホルモンの配合剤投与群では、アルツハイマーを含む認知症の危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:2.05)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、アルツハイマーを含む認知症の危険性がプラセボ投与群と比較して有意ではないが、高い傾向がみられた(ハザード比:1.49)との報告がある10) ,11) 。
- 15.1.6 長期投与により肝腫瘍が発生したとの報告がある。
- 15.1.7 HRTと卵巣癌の危険性
-
15.1.8 HRTと胆嚢疾患の危険性
米国におけるWHI試験の結果、本剤と黄体ホルモンの配合剤投与群において、胆嚢疾患になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.59)との報告がある。並行して行われた子宮摘出者に対する試験の結果、本剤単独投与群では、胆嚢疾患になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.67)との報告がある16) 。