薬効分類名副甲状腺機能低下症治療剤
一般的名称パロペグテリパラチド
ヨビパス皮下注168μgペン、ヨビパス皮下注294μgペン、ヨビパス皮下注420μgペン
よびぱす、よびぱす、よびぱす
YORVIPATH Subcutaneous Injection, YORVIPATH Subcutaneous Injection, YORVIPATH Subcutaneous Injection
製造販売元/帝人ファーマ株式会社
重大な副作用
その他の副作用
併用注意
- ジギタリス製剤
- [8.1 参照],[11.1.1 参照]
高カルシウム血症に伴い不整脈があらわれることがある。
血清カルシウム値が上昇すると、ジギタリスの作用が増強される。
- ビスホスホネート系製剤
- デノスマブ
- ロモソズマブ等
- [8.1 参照],[11.1.1 参照]
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。
- テリパラチド製剤
- [8.1 参照],[11.1.1 参照]
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。
- アバロパラチド酢酸塩製剤
- [8.1 参照],[11.1.1 参照]
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。
- ループ系利尿薬
- サイアザイド系利尿薬
- サイアザイド系類似利尿薬
- [8.1 参照],[11.1.1 参照]
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。
- リチウム製剤
- [8.1 参照],[11.1.1 参照]
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。
2. 禁忌(次の患者には投与しないこと)
本剤の成分に対し過敏症の既往歴のある患者
4. 効能又は効果
副甲状腺機能低下症
5. 効能又は効果に関連する注意
- 5.1 活性型ビタミンD製剤やカルシウム剤による治療を受けている患者に対して、本剤の投与を検討すること。[7.1 参照]
- 5.2 副甲状腺ホルモン分泌不全の患者に対して、本剤の投与を検討すること。偽性副甲状腺機能低下症の患者では、副甲状腺ホルモンに対する反応性が低下しており本剤の効果が期待できないため、本剤の投与前に血中PTH濃度を測定する等、適切に鑑別診断を行うこと。
6. 用法及び用量
通常、成人には、パロペグテリパラチドを、PTH(1-34)として1回18μgを開始用量とし、1日1回、皮下注射する。以後、患者の血清カルシウム濃度の十分な管理のもとに、1日1回6~60μgの範囲で適宜用量を増減して皮下投与するが、増量又は減量は3μgずつ行うこと。
7. 用法及び用量に関連する注意
- 7.1 活性型ビタミンD製剤やカルシウム剤による治療により患者の血清カルシウム濃度が基準範囲内又はわずかに下回る状態(目安として7.8~10.6mg/dL)となっていることを確認した上で、本剤を投与すること。[5.1 参照]
- 7.2 本剤の投与開始時には、以下を参考に活性型ビタミンD製剤及びカルシウム剤の投与量を調節すること。
-
7.3 本剤の初回投与後、及び本剤、活性型ビタミンD製剤又はカルシウム剤の投与量を変更した後は、7~14日後を目安に血清カルシウム濃度を測定し、下図を参考に、血清カルシウム濃度が正常範囲内に維持されるように、本剤、活性型ビタミンD製剤又はカルシウム剤の投与量を調節すること。[8.1 参照],[11.1.1 参照]
図1 本剤、活性型ビタミンD製剤及びカルシウム剤の投与量調節方法 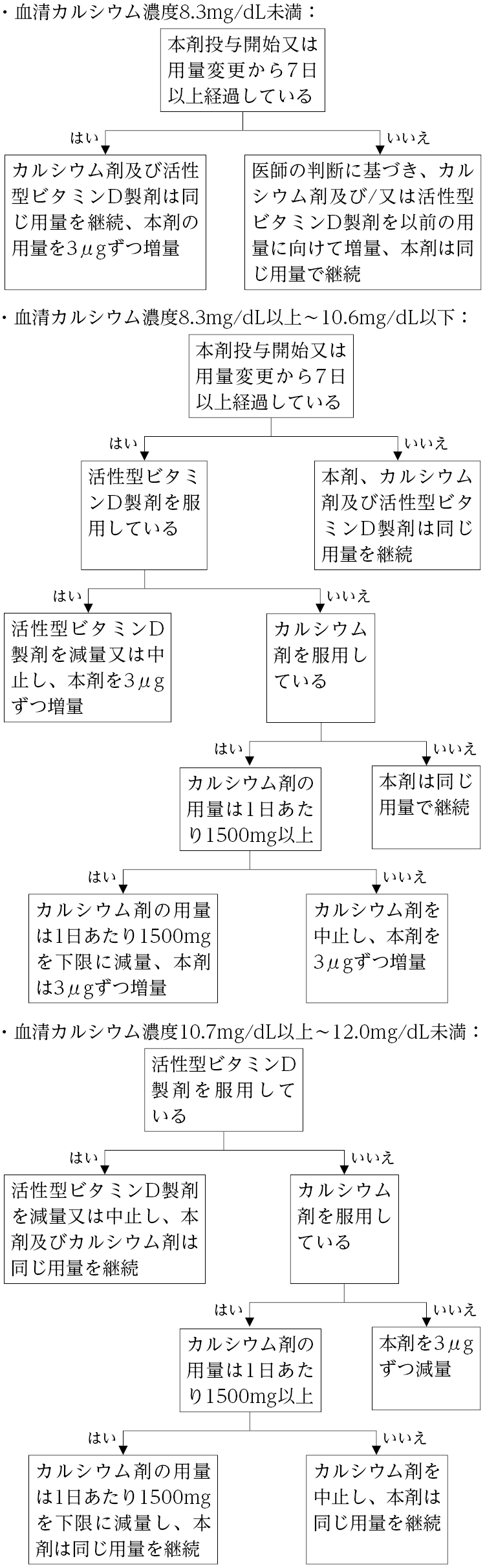
-
7.4 本剤の用量調節にあたっては、以下の点に留意すること。
- 血清カルシウム濃度が12.0mg/dL以上となった場合は、本剤を2~3日間を目安に休薬すること。その後、治療を再開する場合は、血清カルシウム濃度が12.0mg/dL未満となったことを確認した上で、7.3の図を参考に、患者の血清カルシウム濃度及び休薬前の本剤の用量に基づき、本剤、活性型ビタミンD製剤及びカルシウム剤の用量を調節すること。[8.1 参照],[11.1.1 参照]
- 投与を忘れた場合には、気付いた時点で直ちに投与すること。ただし、1日に2回の投与は行わないこと。
- 本剤の投与を3日以上休薬した場合は、低カルシウム血症の徴候・症状がないか確認し、血清カルシウム濃度の測定を検討すること。本剤による治療を再開する場合は、休薬前の用量から投与を開始し、その後は7.3の図を参考に、患者の血清カルシウム濃度に基づき、本剤、活性型ビタミンD製剤及びカルシウム剤の用量を調節すること。
-
7.5 低アルブミン血症(血清アルブミン濃度が4.0g/dL未満)がある場合には、補正カルシウム濃度
注7)
を指標に用量を調節すること。注7) 補正カルシウム濃度(mg/dL)=血清カルシウム濃度(mg/dL)−血清アルブミン濃度(g/dL)+4.0
8. 重要な基本的注意
- 8.1 高カルシウム血症があらわれることがあるので、本剤投与中は定期的に血清カルシウム濃度を測定すること。[7.3 参照],[7.4 参照],[10.2 参照],[11.1.1 参照]
- 8.2 本剤の効果を十分に発揮させるため、ビタミンDが欠乏していない状態で本剤を投与することが望ましい。本剤の投与前及び投与期間中にビタミンD欠乏が疑われる場合は、ビタミンDに関する栄養指導や生活指導等の実施を考慮すること。
- 8.3 起立性低血圧、めまい、立ちくらみ等があらわれることがあるので、高所での作業、自動車の運転等危険が伴う作業に従事する場合には注意させること。
- 8.4 本剤の自己注射にあたっては、以下の点に留意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 骨肉腫発生のリスクが高いと考えられる患者
以下のような骨肉腫発生のリスクが高いと考えられる患者に対しては、患者のベネフィットとリスクを考慮して本剤の投与の可否を検討すること。[15.2.1 参照],[15.2.2 参照]
9.2 腎機能障害患者
-
9.2.1 重度の腎機能障害患者(eGFRが30mL/min/1.73m2未満)
特に投与開始時に高カルシウム血症を起こす可能性があることから、投与開始後は血清カルシウム濃度や患者の状態を十分に観察すること。重度の腎機能障害を有する又は透析中の副甲状腺機能低下症患者を対象とした臨床試験は実施していない。[16.6.1 参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[15.2.3 参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。本剤の乳汁中への移行に関するデータはない。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下している。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
|
高カルシウム血症に伴い不整脈があらわれることがある。 |
血清カルシウム値が上昇すると、ジギタリスの作用が増強される。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
15. その他の注意
15.2 非臨床試験に基づく情報
- 15.2.1 雌雄ラットに本薬を皮下投与した反復投与毒性試験において、2μg/kg/日及び5μg/kg/日(5μg/kg/日投与時の遊離PTHのAUC比はヒトに本剤60μg/日を投与した場合の約2倍)で骨吸収作用を示唆する変化(鼻骨の空隙率の増加等)が、10μg/kg/日以上(遊離PTHのAUC比は、ヒトに本剤60μg/日を投与した場合の約5倍以上)では骨形成作用を示唆する変化(大腿骨・胸骨の骨増加等)が認められた。また、20μg/kg/日(遊離PTHのAUC比はヒトに本剤60μg/日を投与した場合の約9倍)で骨端線の異常(異形成)が認められた1) 。[9.1.1 参照]
- 15.2.2 本薬のがん原性試験は実施されていない。テリパラチド製剤(骨粗鬆症治療剤)では、雌雄ラットに皮下投与したがん原性試験において、骨肉腫を含む骨腫瘍性病変の発生頻度が増加したとの報告がある。[9.1.1 参照]
- 15.2.3 テリパラチド(遺伝子組換え)の動物試験では、ウサギで胎児毒性(胚死亡)が、マウスで胎児の骨格変異又は異常のわずかな増加が、ラットで出生児の体重増加抑制及び自発運動量の低下が認められている。ラットに本薬30μg/kg/日又はウサギに本薬6μg/kg/日(遊離PTHのAUC比は、ヒトに本剤60μg/日を投与した場合と比較して、それぞれ約7.9倍及び6.6倍)を投与した試験では、胚・胎児発生への影響を示唆する所見は認められていない2) 。[9.5 参照]
2. 禁忌(次の患者には投与しないこと)
本剤の成分に対し過敏症の既往歴のある患者
4. 効能又は効果
副甲状腺機能低下症
5. 効能又は効果に関連する注意
- 5.1 活性型ビタミンD製剤やカルシウム剤による治療を受けている患者に対して、本剤の投与を検討すること。[7.1 参照]
- 5.2 副甲状腺ホルモン分泌不全の患者に対して、本剤の投与を検討すること。偽性副甲状腺機能低下症の患者では、副甲状腺ホルモンに対する反応性が低下しており本剤の効果が期待できないため、本剤の投与前に血中PTH濃度を測定する等、適切に鑑別診断を行うこと。
6. 用法及び用量
通常、成人には、パロペグテリパラチドを、PTH(1-34)として1回18μgを開始用量とし、1日1回、皮下注射する。以後、患者の血清カルシウム濃度の十分な管理のもとに、1日1回6~60μgの範囲で適宜用量を増減して皮下投与するが、増量又は減量は3μgずつ行うこと。
7. 用法及び用量に関連する注意
- 7.1 活性型ビタミンD製剤やカルシウム剤による治療により患者の血清カルシウム濃度が基準範囲内又はわずかに下回る状態(目安として7.8~10.6mg/dL)となっていることを確認した上で、本剤を投与すること。[5.1 参照]
- 7.2 本剤の投与開始時には、以下を参考に活性型ビタミンD製剤及びカルシウム剤の投与量を調節すること。
-
7.3 本剤の初回投与後、及び本剤、活性型ビタミンD製剤又はカルシウム剤の投与量を変更した後は、7~14日後を目安に血清カルシウム濃度を測定し、下図を参考に、血清カルシウム濃度が正常範囲内に維持されるように、本剤、活性型ビタミンD製剤又はカルシウム剤の投与量を調節すること。[8.1 参照],[11.1.1 参照]
図1 本剤、活性型ビタミンD製剤及びカルシウム剤の投与量調節方法 
-
7.4 本剤の用量調節にあたっては、以下の点に留意すること。
- 血清カルシウム濃度が12.0mg/dL以上となった場合は、本剤を2~3日間を目安に休薬すること。その後、治療を再開する場合は、血清カルシウム濃度が12.0mg/dL未満となったことを確認した上で、7.3の図を参考に、患者の血清カルシウム濃度及び休薬前の本剤の用量に基づき、本剤、活性型ビタミンD製剤及びカルシウム剤の用量を調節すること。[8.1 参照],[11.1.1 参照]
- 投与を忘れた場合には、気付いた時点で直ちに投与すること。ただし、1日に2回の投与は行わないこと。
- 本剤の投与を3日以上休薬した場合は、低カルシウム血症の徴候・症状がないか確認し、血清カルシウム濃度の測定を検討すること。本剤による治療を再開する場合は、休薬前の用量から投与を開始し、その後は7.3の図を参考に、患者の血清カルシウム濃度に基づき、本剤、活性型ビタミンD製剤及びカルシウム剤の用量を調節すること。
-
7.5 低アルブミン血症(血清アルブミン濃度が4.0g/dL未満)がある場合には、補正カルシウム濃度
注7)
を指標に用量を調節すること。注7) 補正カルシウム濃度(mg/dL)=血清カルシウム濃度(mg/dL)−血清アルブミン濃度(g/dL)+4.0
8. 重要な基本的注意
- 8.1 高カルシウム血症があらわれることがあるので、本剤投与中は定期的に血清カルシウム濃度を測定すること。[7.3 参照],[7.4 参照],[10.2 参照],[11.1.1 参照]
- 8.2 本剤の効果を十分に発揮させるため、ビタミンDが欠乏していない状態で本剤を投与することが望ましい。本剤の投与前及び投与期間中にビタミンD欠乏が疑われる場合は、ビタミンDに関する栄養指導や生活指導等の実施を考慮すること。
- 8.3 起立性低血圧、めまい、立ちくらみ等があらわれることがあるので、高所での作業、自動車の運転等危険が伴う作業に従事する場合には注意させること。
- 8.4 本剤の自己注射にあたっては、以下の点に留意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 骨肉腫発生のリスクが高いと考えられる患者
以下のような骨肉腫発生のリスクが高いと考えられる患者に対しては、患者のベネフィットとリスクを考慮して本剤の投与の可否を検討すること。[15.2.1 参照],[15.2.2 参照]
9.2 腎機能障害患者
-
9.2.1 重度の腎機能障害患者(eGFRが30mL/min/1.73m2未満)
特に投与開始時に高カルシウム血症を起こす可能性があることから、投与開始後は血清カルシウム濃度や患者の状態を十分に観察すること。重度の腎機能障害を有する又は透析中の副甲状腺機能低下症患者を対象とした臨床試験は実施していない。[16.6.1 参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[15.2.3 参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。本剤の乳汁中への移行に関するデータはない。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下している。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
|
高カルシウム血症に伴い不整脈があらわれることがある。 |
血清カルシウム値が上昇すると、ジギタリスの作用が増強される。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
|
|
本剤による血清カルシウム濃度の正常化が阻害され、本剤の治療効果に影響を与える可能性がある。 |
これらの薬剤は血清カルシウムや骨代謝に影響を及ぼし、本剤の治療効果に影響を与える可能性がある。 |
15. その他の注意
15.2 非臨床試験に基づく情報
- 15.2.1 雌雄ラットに本薬を皮下投与した反復投与毒性試験において、2μg/kg/日及び5μg/kg/日(5μg/kg/日投与時の遊離PTHのAUC比はヒトに本剤60μg/日を投与した場合の約2倍)で骨吸収作用を示唆する変化(鼻骨の空隙率の増加等)が、10μg/kg/日以上(遊離PTHのAUC比は、ヒトに本剤60μg/日を投与した場合の約5倍以上)では骨形成作用を示唆する変化(大腿骨・胸骨の骨増加等)が認められた。また、20μg/kg/日(遊離PTHのAUC比はヒトに本剤60μg/日を投与した場合の約9倍)で骨端線の異常(異形成)が認められた1) 。[9.1.1 参照]
- 15.2.2 本薬のがん原性試験は実施されていない。テリパラチド製剤(骨粗鬆症治療剤)では、雌雄ラットに皮下投与したがん原性試験において、骨肉腫を含む骨腫瘍性病変の発生頻度が増加したとの報告がある。[9.1.1 参照]
- 15.2.3 テリパラチド(遺伝子組換え)の動物試験では、ウサギで胎児毒性(胚死亡)が、マウスで胎児の骨格変異又は異常のわずかな増加が、ラットで出生児の体重増加抑制及び自発運動量の低下が認められている。ラットに本薬30μg/kg/日又はウサギに本薬6μg/kg/日(遊離PTHのAUC比は、ヒトに本剤60μg/日を投与した場合と比較して、それぞれ約7.9倍及び6.6倍)を投与した試験では、胚・胎児発生への影響を示唆する所見は認められていない2) 。[9.5 参照]