薬効分類名経皮吸収型・β₁遮断剤
一般的名称ビソプロロール・テープ剤
ビソノテープ2mg、ビソノテープ4mg、ビソノテープ8mg
びそのてーぷ2mg、びそのてーぷ4mg、びそのてーぷ8mg
Bisono Tapes 2mg, Bisono Tapes 4mg, Bisono Tapes 8mg
製造販売元/トーアエイヨー株式会社
重大な副作用
その他の副作用
併用注意
交感神経系に対し抑制的に作用する薬剤
- レセルピン 等
過剰の交感神経抑制作用(徐脈、血圧低下等)があらわれることがある。
相加的に作用(交感神経抑制作用)を増強させる。
血糖降下剤
- インスリン製剤
- トルブタミド 等
血糖降下作用が増強することがある。また、低血糖症状(頻脈、発汗等)をマスクすることがある。
β2遮断により肝臓でのグリコーゲン分解が抑制される。また、低血糖時に分泌されるアドレナリンにより生じる低血糖症状をマスクする。
Ca拮抗剤
- ベラパミル塩酸塩
- ジルチアゼム塩酸塩 等
徐脈、房室ブロック、洞房ブロック等があらわれることがある。
相加的に作用(心刺激生成・伝導抑制作用、陰性変力作用、降圧作用)を増強させる。特にジギタリス製剤との3剤併用時には注意を要する。
ジギタリス製剤
- ジゴキシン
- メチルジゴキシン
徐脈、房室ブロック等があらわれることがある。
相加的に作用(心刺激生成・伝導抑制作用)を増強させる。特にCa拮抗剤との3剤併用時には注意を要する。
クロニジン塩酸塩
グアナベンズ酢酸塩
クロニジン、グアナベンズ投与中止後のリバウンド現象(急激な血圧上昇)が増強することがある。
クロニジンを中止した場合、血中ノルアドレナリンが上昇する。β遮断剤と併用している場合、クロニジンの中止により、α作用が強調され、より急激な血圧上昇を起こす。グアナベンズも作用機序から同様な反応が予測される。
クラスⅠ抗不整脈剤
- ジソピラミドリン酸塩
- プロカインアミド塩酸塩
- アジマリン 等
クラスⅢ抗不整脈剤
- アミオダロン塩酸塩
過度の心機能抑制(徐脈、低血圧等)があらわれることがある。
相加的に作用(交感神経抑制作用)を増強させる。
非ステロイド性抗炎症剤
- インドメタシン 等
本剤の降圧作用が減弱することがある。
非ステロイド性抗炎症剤は、血管拡張作用を有するプロスタグランジンの合成・遊離を阻害する。
降圧作用を有する薬剤
- 降圧剤
- 硝酸剤
降圧作用が増強することがある。
相加的に作用(降圧作用)を増強させる。
フィンゴリモド塩酸塩
フィンゴリモド塩酸塩の投与開始時に併用すると重度の徐脈や心ブロックが認められることがある。
共に徐脈や心ブロックを引き起こすおそれがある。
2. 禁忌(次の患者には投与しないこと)
-
2.1 高度の徐脈(著しい洞性徐脈)、房室ブロック(Ⅱ、Ⅲ度)、洞房ブロック、洞不全症候群のある患者
[症状を悪化させるおそれがある。]
-
2.2 糖尿病性ケトアシドーシス、代謝性アシドーシスのある患者
[アシドーシスに基づく心収縮力の抑制を増強させるおそれがある。]
-
2.3 心原性ショックのある患者
[心機能が抑制され、症状を悪化させるおそれがある。]
-
2.4 肺高血圧による右心不全のある患者
[心機能が抑制され、症状を悪化させるおそれがある。]
-
2.5 強心薬又は血管拡張薬を静脈内投与する必要のある心不全患者
[心収縮力抑制作用により、心不全が悪化するおそれがある。]
-
2.6 非代償性の心不全患者
[心収縮力抑制作用により、心不全が悪化するおそれがある。]
-
2.7 重度の末梢循環障害のある患者(壊疽等)
[末梢血管の拡張を抑制し、症状を悪化させるおそれがある。]
- 2.8 未治療の褐色細胞腫又はパラガングリオーマの患者[7.1 参照],[9.1.11 参照]
- 2.9 本剤の成分に対し過敏症の既往歴のある患者
7. 用法及び用量に関連する注意
- 7.1 褐色細胞腫又はパラガングリオーマの患者では、α遮断剤で初期治療を行った後に本剤を投与し、常にα遮断剤を併用すること。[2.8 参照],[9.1.11 参照]
- 7.2 頻脈性心房細動を合併する本態性高血圧症の患者に投与する場合、頻脈性心房細動の用法及び用量は1日1回4mgから開始することに留意した上で、各疾患の指標となる血圧や心拍数、症状等に応じ、開始用量を設定すること。
8. 重要な基本的注意
- 8.1 投与が長期にわたる場合は、心機能検査(脈拍、血圧、心電図、X線等)を定期的に行うこと。徐脈又は低血圧の症状があらわれた場合には減量又は投与を中止すること。また、必要に応じアトロピンを使用すること。なお、肝機能、腎機能、血液像等に注意すること。
- 8.2 類似化合物(プロプラノロール塩酸塩)使用中の狭心症患者で急に投与を中止したとき、症状が悪化したり、心筋梗塞を起こした症例が報告されているので、休薬を要する場合は徐々に減量し、観察を十分に行うこと。また、患者に医師の指示なしに使用を中止しないよう注意すること。特に高齢者においては同様の注意をすること。[9.8.2 参照]
- 8.3 手術前48時間は投与しないことが望ましい。
- 8.4 めまい、ふらつきがあらわれることがあるので、本剤投与中の患者(特に投与初期)には自動車の運転等危険を伴う機械を操作する際には注意させること。
- 8.5 本剤の貼付により皮膚症状を起こすことがあるので、本剤の使用が適切であるか慎重に判断すること。また、本剤の貼付に際しては貼付部位を毎回変更すること。皮膚症状があらわれた場合には、ステロイド軟膏等を投与するか、本剤を投与中止するなど適切な処置を行うこと。[14.1.1 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 気管支喘息、気管支痙攣のおそれのある患者
気管支を収縮させ、症状を発現させるおそれがある。
-
9.1.2 心不全を合併する患者
心機能検査を行う等、観察を十分に行うこと。症状を悪化させるおそれがある。
-
9.1.3 うっ血性心不全のおそれのある患者
観察を十分に行うこと。心機能が抑制され、症状を悪化させるおそれがある。
-
9.1.4 特発性低血糖症、コントロール不十分な糖尿病、長期間絶食状態の患者
血糖値に注意すること。低血糖の前駆症状である頻脈等の交感神経系反応をマスクしやすい。
-
9.1.5 甲状腺中毒症の患者
休薬を要する場合には徐々に減量し、観察を十分に行うこと。急に投与を中止すると、症状を悪化させるおそれがある。また、頻脈等の中毒症状をマスクすることがある。
-
9.1.6 末梢循環障害のある患者(レイノー症候群、間欠性跛行症等)
末梢血管の拡張を抑制し、症状を悪化させるおそれがある。
-
9.1.7 徐脈、房室ブロック(Ⅰ度)のある患者
心刺激伝導系を抑制し、症状を悪化させるおそれがある。
-
9.1.8 過度に血圧の低い患者
血圧を更に低下させるおそれがある。
-
9.1.9 異型狭心症の患者
症状を悪化させるおそれがある。
-
9.1.10 乾癬の患者又は乾癬の既往のある患者
症状を悪化又は誘発させるおそれがある。
- 9.1.11 褐色細胞腫又はパラガングリオーマの患者
9.2 腎機能障害患者
低用量から投与を開始することを考慮すること。薬物の排泄遅延により血中濃度が上昇し、作用が増強するおそれがある。[16.6.1 参照]
9.5 妊婦
*妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与に際しては、母体及び胎児の状態を十分に観察すること。また、出生後も新生児の状態を十分に観察し、新生児の低血糖、徐脈、哺乳不良等の異常が認められた場合には適切な処置を行うこと。
*妊婦にβ遮断薬を投与した場合に、胎児の発育不全、新生児の低血糖、徐脈、哺乳不良等が認められたとの報告がある。また、動物実験(ラット、ウサギ)で胎児毒性(致死、発育抑制)及び新生児毒性(発育毒性等)が報告されている(安全域 注1) :ラット胎児で58倍、ウサギ胎児で39倍、ラット新生児で19倍)。
*
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
- 9.8.1 少量から投与を開始するなど患者の状態を観察しながら慎重に投与すること。一般に過度の降圧は好ましくないとされている。また、脳梗塞等がおこるおそれがある。
- 9.8.2 徐脈等の心拍数・心リズム障害があらわれやすいので、このような症状があらわれた場合には減量又は投与を中止すること。なお、休薬を要する場合は、徐々に減量する。[8.2 参照]
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
過剰の交感神経抑制作用(徐脈、血圧低下等)があらわれることがある。 異常が認められた場合には両剤の減量若しくは投与を中止する。 |
相加的に作用(交感神経抑制作用)を増強させる。 |
|
血糖降下作用が増強することがある。また、低血糖症状(頻脈、発汗等)をマスクすることがある。 血糖値に注意し、異常が認められた場合には本剤の減量若しくは投与を中止する。 |
β2遮断により肝臓でのグリコーゲン分解が抑制される。また、低血糖時に分泌されるアドレナリンにより生じる低血糖症状をマスクする。 |
|
徐脈、房室ブロック、洞房ブロック等があらわれることがある。 定期的に脈拍数を測定し、必要に応じて心電図検査を行い、異常が認められた場合には、両剤の減量若しくは投与を中止する。 |
相加的に作用(心刺激生成・伝導抑制作用、陰性変力作用、降圧作用)を増強させる。特にジギタリス製剤との3剤併用時には注意を要する。 |
|
徐脈、房室ブロック等があらわれることがある。 定期的に心電図検査を行い、異常が認められた場合には、両剤の減量若しくは投与を中止する。 |
相加的に作用(心刺激生成・伝導抑制作用)を増強させる。特にCa拮抗剤との3剤併用時には注意を要する。 |
|
クロニジン塩酸塩 グアナベンズ酢酸塩 |
クロニジン、グアナベンズ投与中止後のリバウンド現象(急激な血圧上昇)が増強することがある。 クロニジンを中止する場合は、あらかじめ本剤の投与中止等適切な処置を行う。 |
クロニジンを中止した場合、血中ノルアドレナリンが上昇する。β遮断剤と併用している場合、クロニジンの中止により、α作用が強調され、より急激な血圧上昇を起こす。グアナベンズも作用機序から同様な反応が予測される。 |
過度の心機能抑制(徐脈、低血圧等)があらわれることがある。 臨床症状を観察し、異常が認められた場合には本剤の減量若しくは投与を中止する。 |
相加的に作用(交感神経抑制作用)を増強させる。 |
|
本剤の降圧作用が減弱することがある。 |
非ステロイド性抗炎症剤は、血管拡張作用を有するプロスタグランジンの合成・遊離を阻害する。 |
|
降圧作用が増強することがある。 定期的に血圧を測定し、両剤の用量を調節する。 |
相加的に作用(降圧作用)を増強させる。 |
|
フィンゴリモド塩酸塩 |
フィンゴリモド塩酸塩の投与開始時に併用すると重度の徐脈や心ブロックが認められることがある。 |
共に徐脈や心ブロックを引き起こすおそれがある。 |
11. 副作用
11.1 重大な副作用
11.2 その他の副作用
1%以上 |
1%未満 注2) |
頻度不明 注3) |
|
|---|---|---|---|
循環器 |
徐脈 |
房室ブロック、血圧低下、心室性期外収縮、動悸、胸痛 |
心房細動、心胸郭比増加 |
精神神経系 |
頭痛、傾眠、浮動性めまい、体位性めまい |
頭重感、不眠、悪夢 |
|
消化器 |
悪心、嘔吐、胃部不快感、腹部不快感、食欲不振、下痢 |
||
肝臓 |
ALTの上昇 |
AST、LDH、Al-P、ビリルビンの上昇 |
γ-GTPの上昇、肝腫大 |
腎臓・泌尿器 |
尿中蛋白陽性 |
クレアチニン、BUNの上昇 |
尿中ブドウ糖陽性、頻尿 |
呼吸器 |
呼吸困難 |
気管支痙攣 |
|
過敏症 |
皮膚そう痒感 |
発疹 |
|
眼 |
霧視、涙液分泌減少 |
||
適用部位障害 |
(適用部位) 皮膚炎、紅斑、そう痒感 |
(適用部位) 疼痛、熱感、乾燥、湿疹、変色、びらん |
|
その他 |
好酸球百分率増加、血中トリグリセリド増加、血中尿酸増加、CRP増加 |
無力症、疲労、倦怠感、CKの上昇、血中コレステロール増加、HDLコレステロール増加、LDLコレステロール増加、血中ブドウ糖増加 |
浮腫、気分不快感、四肢冷感、悪寒、しびれ感、糖尿病増悪 |
14. 適用上の注意
14.1 薬剤交付時の注意
患者に対し以下の点に注意するよう指導すること。
-
14.1.1 貼付部位
- 皮膚の損傷又は湿疹・皮膚炎等がみられる部位には貼付しないこと。
- 貼付部位に、発汗、湿潤、汚染等がみられるときは清潔なタオル等でよくふき取ってから本剤を貼付すること。特に夏期は、一般的に密封療法では皮膚症状が誘発されることが知られているので、十分に注意して投与すること。
- 皮膚刺激を避けるため、毎回貼付部位を変えること。[8.5 参照]
-
14.1.2 貼付期間中
本剤が皮膚から一部剥離した場合は、絆創膏等で剥離部を固定すること。
-
14.1.3 保管
使用するまではアルミ袋を開封しないこと。
2. 禁忌(次の患者には投与しないこと)
-
2.1 高度の徐脈(著しい洞性徐脈)、房室ブロック(Ⅱ、Ⅲ度)、洞房ブロック、洞不全症候群のある患者
[症状を悪化させるおそれがある。]
-
2.2 糖尿病性ケトアシドーシス、代謝性アシドーシスのある患者
[アシドーシスに基づく心収縮力の抑制を増強させるおそれがある。]
-
2.3 心原性ショックのある患者
[心機能が抑制され、症状を悪化させるおそれがある。]
-
2.4 肺高血圧による右心不全のある患者
[心機能が抑制され、症状を悪化させるおそれがある。]
-
2.5 強心薬又は血管拡張薬を静脈内投与する必要のある心不全患者
[心収縮力抑制作用により、心不全が悪化するおそれがある。]
-
2.6 非代償性の心不全患者
[心収縮力抑制作用により、心不全が悪化するおそれがある。]
-
2.7 重度の末梢循環障害のある患者(壊疽等)
[末梢血管の拡張を抑制し、症状を悪化させるおそれがある。]
- 2.8 未治療の褐色細胞腫又はパラガングリオーマの患者[7.1 参照],[9.1.11 参照]
- 2.9 本剤の成分に対し過敏症の既往歴のある患者
7. 用法及び用量に関連する注意
- 7.1 褐色細胞腫又はパラガングリオーマの患者では、α遮断剤で初期治療を行った後に本剤を投与し、常にα遮断剤を併用すること。[2.8 参照],[9.1.11 参照]
- 7.2 頻脈性心房細動を合併する本態性高血圧症の患者に投与する場合、頻脈性心房細動の用法及び用量は1日1回4mgから開始することに留意した上で、各疾患の指標となる血圧や心拍数、症状等に応じ、開始用量を設定すること。
8. 重要な基本的注意
- 8.1 投与が長期にわたる場合は、心機能検査(脈拍、血圧、心電図、X線等)を定期的に行うこと。徐脈又は低血圧の症状があらわれた場合には減量又は投与を中止すること。また、必要に応じアトロピンを使用すること。なお、肝機能、腎機能、血液像等に注意すること。
- 8.2 類似化合物(プロプラノロール塩酸塩)使用中の狭心症患者で急に投与を中止したとき、症状が悪化したり、心筋梗塞を起こした症例が報告されているので、休薬を要する場合は徐々に減量し、観察を十分に行うこと。また、患者に医師の指示なしに使用を中止しないよう注意すること。特に高齢者においては同様の注意をすること。[9.8.2 参照]
- 8.3 手術前48時間は投与しないことが望ましい。
- 8.4 めまい、ふらつきがあらわれることがあるので、本剤投与中の患者(特に投与初期)には自動車の運転等危険を伴う機械を操作する際には注意させること。
- 8.5 本剤の貼付により皮膚症状を起こすことがあるので、本剤の使用が適切であるか慎重に判断すること。また、本剤の貼付に際しては貼付部位を毎回変更すること。皮膚症状があらわれた場合には、ステロイド軟膏等を投与するか、本剤を投与中止するなど適切な処置を行うこと。[14.1.1 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 気管支喘息、気管支痙攣のおそれのある患者
気管支を収縮させ、症状を発現させるおそれがある。
-
9.1.2 心不全を合併する患者
心機能検査を行う等、観察を十分に行うこと。症状を悪化させるおそれがある。
-
9.1.3 うっ血性心不全のおそれのある患者
観察を十分に行うこと。心機能が抑制され、症状を悪化させるおそれがある。
-
9.1.4 特発性低血糖症、コントロール不十分な糖尿病、長期間絶食状態の患者
血糖値に注意すること。低血糖の前駆症状である頻脈等の交感神経系反応をマスクしやすい。
-
9.1.5 甲状腺中毒症の患者
休薬を要する場合には徐々に減量し、観察を十分に行うこと。急に投与を中止すると、症状を悪化させるおそれがある。また、頻脈等の中毒症状をマスクすることがある。
-
9.1.6 末梢循環障害のある患者(レイノー症候群、間欠性跛行症等)
末梢血管の拡張を抑制し、症状を悪化させるおそれがある。
-
9.1.7 徐脈、房室ブロック(Ⅰ度)のある患者
心刺激伝導系を抑制し、症状を悪化させるおそれがある。
-
9.1.8 過度に血圧の低い患者
血圧を更に低下させるおそれがある。
-
9.1.9 異型狭心症の患者
症状を悪化させるおそれがある。
-
9.1.10 乾癬の患者又は乾癬の既往のある患者
症状を悪化又は誘発させるおそれがある。
- 9.1.11 褐色細胞腫又はパラガングリオーマの患者
9.2 腎機能障害患者
低用量から投与を開始することを考慮すること。薬物の排泄遅延により血中濃度が上昇し、作用が増強するおそれがある。[16.6.1 参照]
9.5 妊婦
*妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与に際しては、母体及び胎児の状態を十分に観察すること。また、出生後も新生児の状態を十分に観察し、新生児の低血糖、徐脈、哺乳不良等の異常が認められた場合には適切な処置を行うこと。
*妊婦にβ遮断薬を投与した場合に、胎児の発育不全、新生児の低血糖、徐脈、哺乳不良等が認められたとの報告がある。また、動物実験(ラット、ウサギ)で胎児毒性(致死、発育抑制)及び新生児毒性(発育毒性等)が報告されている(安全域 注1) :ラット胎児で58倍、ウサギ胎児で39倍、ラット新生児で19倍)。
*
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
- 9.8.1 少量から投与を開始するなど患者の状態を観察しながら慎重に投与すること。一般に過度の降圧は好ましくないとされている。また、脳梗塞等がおこるおそれがある。
- 9.8.2 徐脈等の心拍数・心リズム障害があらわれやすいので、このような症状があらわれた場合には減量又は投与を中止すること。なお、休薬を要する場合は、徐々に減量する。[8.2 参照]
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
過剰の交感神経抑制作用(徐脈、血圧低下等)があらわれることがある。 異常が認められた場合には両剤の減量若しくは投与を中止する。 |
相加的に作用(交感神経抑制作用)を増強させる。 |
|
血糖降下作用が増強することがある。また、低血糖症状(頻脈、発汗等)をマスクすることがある。 血糖値に注意し、異常が認められた場合には本剤の減量若しくは投与を中止する。 |
β2遮断により肝臓でのグリコーゲン分解が抑制される。また、低血糖時に分泌されるアドレナリンにより生じる低血糖症状をマスクする。 |
|
徐脈、房室ブロック、洞房ブロック等があらわれることがある。 定期的に脈拍数を測定し、必要に応じて心電図検査を行い、異常が認められた場合には、両剤の減量若しくは投与を中止する。 |
相加的に作用(心刺激生成・伝導抑制作用、陰性変力作用、降圧作用)を増強させる。特にジギタリス製剤との3剤併用時には注意を要する。 |
|
徐脈、房室ブロック等があらわれることがある。 定期的に心電図検査を行い、異常が認められた場合には、両剤の減量若しくは投与を中止する。 |
相加的に作用(心刺激生成・伝導抑制作用)を増強させる。特にCa拮抗剤との3剤併用時には注意を要する。 |
|
クロニジン塩酸塩 グアナベンズ酢酸塩 |
クロニジン、グアナベンズ投与中止後のリバウンド現象(急激な血圧上昇)が増強することがある。 クロニジンを中止する場合は、あらかじめ本剤の投与中止等適切な処置を行う。 |
クロニジンを中止した場合、血中ノルアドレナリンが上昇する。β遮断剤と併用している場合、クロニジンの中止により、α作用が強調され、より急激な血圧上昇を起こす。グアナベンズも作用機序から同様な反応が予測される。 |
過度の心機能抑制(徐脈、低血圧等)があらわれることがある。 臨床症状を観察し、異常が認められた場合には本剤の減量若しくは投与を中止する。 |
相加的に作用(交感神経抑制作用)を増強させる。 |
|
本剤の降圧作用が減弱することがある。 |
非ステロイド性抗炎症剤は、血管拡張作用を有するプロスタグランジンの合成・遊離を阻害する。 |
|
降圧作用が増強することがある。 定期的に血圧を測定し、両剤の用量を調節する。 |
相加的に作用(降圧作用)を増強させる。 |
|
フィンゴリモド塩酸塩 |
フィンゴリモド塩酸塩の投与開始時に併用すると重度の徐脈や心ブロックが認められることがある。 |
共に徐脈や心ブロックを引き起こすおそれがある。 |
11. 副作用
11.1 重大な副作用
11.2 その他の副作用
1%以上 |
1%未満 注2) |
頻度不明 注3) |
|
|---|---|---|---|
循環器 |
徐脈 |
房室ブロック、血圧低下、心室性期外収縮、動悸、胸痛 |
心房細動、心胸郭比増加 |
精神神経系 |
頭痛、傾眠、浮動性めまい、体位性めまい |
頭重感、不眠、悪夢 |
|
消化器 |
悪心、嘔吐、胃部不快感、腹部不快感、食欲不振、下痢 |
||
肝臓 |
ALTの上昇 |
AST、LDH、Al-P、ビリルビンの上昇 |
γ-GTPの上昇、肝腫大 |
腎臓・泌尿器 |
尿中蛋白陽性 |
クレアチニン、BUNの上昇 |
尿中ブドウ糖陽性、頻尿 |
呼吸器 |
呼吸困難 |
気管支痙攣 |
|
過敏症 |
皮膚そう痒感 |
発疹 |
|
眼 |
霧視、涙液分泌減少 |
||
適用部位障害 |
(適用部位) 皮膚炎、紅斑、そう痒感 |
(適用部位) 疼痛、熱感、乾燥、湿疹、変色、びらん |
|
その他 |
好酸球百分率増加、血中トリグリセリド増加、血中尿酸増加、CRP増加 |
無力症、疲労、倦怠感、CKの上昇、血中コレステロール増加、HDLコレステロール増加、LDLコレステロール増加、血中ブドウ糖増加 |
浮腫、気分不快感、四肢冷感、悪寒、しびれ感、糖尿病増悪 |
14. 適用上の注意
14.1 薬剤交付時の注意
患者に対し以下の点に注意するよう指導すること。
-
14.1.1 貼付部位
- 皮膚の損傷又は湿疹・皮膚炎等がみられる部位には貼付しないこと。
- 貼付部位に、発汗、湿潤、汚染等がみられるときは清潔なタオル等でよくふき取ってから本剤を貼付すること。特に夏期は、一般的に密封療法では皮膚症状が誘発されることが知られているので、十分に注意して投与すること。
- 皮膚刺激を避けるため、毎回貼付部位を変えること。[8.5 参照]
-
14.1.2 貼付期間中
本剤が皮膚から一部剥離した場合は、絆創膏等で剥離部を固定すること。
-
14.1.3 保管
使用するまではアルミ袋を開封しないこと。
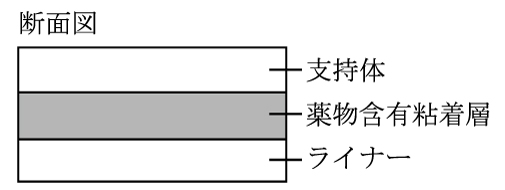
 643(アルミ袋に表示)
643(アルミ袋に表示)