薬効分類名A型ボツリヌス毒素製剤
一般的名称インコボツリヌストキシンA
ゼオマイン注用50単位、ゼオマイン注用100単位、ゼオマイン注用200単位
ぜおまいん、ぜおまいん、ぜおまいん
XEOMIN 50 units for injection, XEOMIN 100 units for injection, XEOMIN 200 units for injection
製造販売元(輸入元)/帝人ファーマ株式会社
重大な副作用
その他の副作用
併用注意
- 筋弛緩剤
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。
- 筋弛緩作用を有する薬剤
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。
- 唾液分泌抑制作用を有する薬剤
慢性流涎患者においては、過剰な唾液分泌抑制があらわれるおそれがあり、口内乾燥、嚥下障害等の発現するリスクが高まるおそれがある。
本剤及びこれらの薬剤はともに唾液分泌抑制作用を有するため作用が増強されるおそれがある。
5. 効能又は効果に関連する注意
- 〈上肢痙縮、下肢痙縮〉
-
〈慢性流涎〉
- 5.4 *神経・筋疾患が原因となる慢性の流涎を有する患者に使用すること。
- 5.5 *臨床試験に組み入れられた患者の原疾患、重症度等の背景及び試験結果を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.3 参照],[17.1.4 参照]
- 5.6 *慢性流涎の原因となる疾患の診断及び治療を併せて行うこと。
6. 用法及び用量
-
〈上肢痙縮〉
通常、成人にはインコボツリヌストキシンAとして複数の緊張筋 注7) に合計400単位を分割して筋肉内注射する。1回あたりの最大投与量は400単位であるが、対象となる緊張筋の種類や数により、投与量は必要最小限となるよう適宜減量する。また、再投与は前回の効果が減弱した場合に可能であるが、投与間隔は12週以上とすること。なお、症状に応じて投与間隔は10週まで短縮できる。
注7) 緊張筋:橈側手根屈筋、尺側手根屈筋、浅指屈筋、深指屈筋、腕橈骨筋、上腕二頭筋、上腕筋、方形回内筋、円回内筋、長母指屈筋、母指内転筋、短母指屈筋/母指対立筋等 -
〈下肢痙縮〉
通常、成人にはインコボツリヌストキシンAとして複数の緊張筋 注8) に合計400単位を分割して筋肉内注射する。1回あたりの最大投与量は400単位であるが、対象となる緊張筋の種類や数により、投与量は必要最小限となるよう適宜減量する。また、再投与は前回の効果が減弱した場合に可能であるが、投与間隔は12週以上とすること。なお、症状に応じて投与間隔は10週まで短縮できる。
注8) 緊張筋:腓腹筋(内側頭、外側頭)、ヒラメ筋、後脛骨筋、長趾屈筋、長母趾屈筋等 -
〈慢性流涎〉
*通常、成人にはインコボツリヌストキシンAとして合計100単位を分割して両側の耳下腺(片側につき30単位)及び顎下腺(片側につき20単位)に注射するが、患者の状態により適宜減量する。また、再投与は前回の効果が減弱した場合に可能であるが、投与間隔は16週以上とすること。なお、患者の状態により投与間隔は14週まで短縮できる。
7. 用法及び用量に関連する注意
-
〈効能共通〉
-
7.1 *複数の適応に本剤を同時投与する場合には、それぞれの効能又は効果で規定されている投与量の上限及び投与間隔を厳守すること。
- 上肢痙縮及び下肢痙縮に対する同時投与では、合計で800単位を上限とし、患者の状態に応じて徐々に増量する等、慎重に投与すること。海外臨床試験において、上肢痙縮及び下肢痙縮に400単位から200単位ずつ増量し、合計800単位までを同時に投与した経験はあるが1) 、国内臨床試験では、上肢痙縮及び下肢痙縮に本剤を同時投与した経験はない。
- *上肢痙縮又は下肢痙縮と、慢性流涎に対して本剤を同時投与した経験はないため、同時投与は避けること。
- 7.2 本剤の力価(単位)は、A型ボツリヌス毒素製剤特有のもので、B型ボツリヌス毒素製剤とは異なること、また換算もできないことに留意し、必ず本剤の投与量を慎重に確認してから投与すること。
- 7.3 他のA型又はB型ボツリヌス毒素製剤を投与後に本剤を使用する場合には、少なくとも他のA型及びB型ボツリヌス毒素製剤の用法及び用量で規定されている投与間隔をあけるとともに、患者の症状を十分に観察した上で、効果が消失し、安全性上の問題がないと判断された場合にのみ投与すること。他のA型及びB型ボツリヌス毒素製剤の投与後12週以内に本剤を投与した場合の安全性及び有効性は確立していない。[10.2 参照]
-
7.1 *複数の適応に本剤を同時投与する場合には、それぞれの効能又は効果で規定されている投与量の上限及び投与間隔を厳守すること。
-
〈上肢痙縮、下肢痙縮〉
- 7.4 本剤と他のA型及びB型ボツリヌス毒素製剤の同時投与は原則として避けること。本剤と他のA型及びB型ボツリヌス毒素製剤を同時投与した際の、安全性及び有効性は確立していない。[10.2 参照]
- 7.5 緊張筋の同定が困難な場合には、筋電計、超音波検査やスティミュレーター等を用いて注意深く目標とする部位を同定すること。
-
7.6 筋ごとの適切な部位及び投与量に留意すること。臨床成績等から、以下のような投与筋、投与量及び投与部位数が推奨されている。[14.2.2 参照]
-
〈上肢痙縮〉
投与筋
投与部位数
(部位/筋)手関節の屈曲
橈側手根屈筋
25-100
1-2
尺側手根屈筋
20-100
1-2
手指関節の屈曲
浅指屈筋
25-100
1-2
深指屈筋
25-100
1-2
肘関節の屈曲
腕橈骨筋
25-100
1-3
上腕二頭筋
50-200
2-4
上腕筋
25-100
1-2
前腕の回内
方形回内筋
10-50
1
円回内筋
25-75
1-2
母指関節の屈曲
長母指屈筋
10-50
1
母指内転筋
5-30
1
短母指屈筋又は母指対立筋
5-30
1
注9) 医師の判断により合計で最大400単位を配分注10) 投与部位一カ所につき最大1.0mLが推奨されている。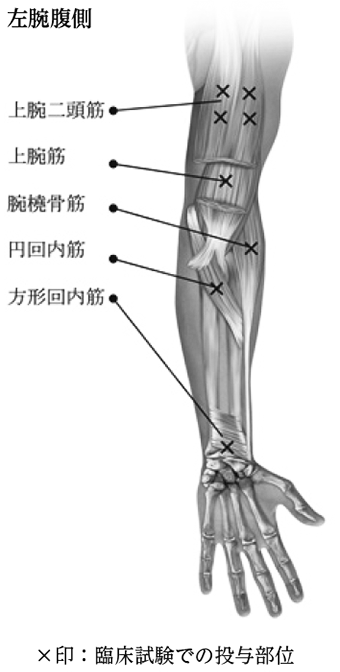
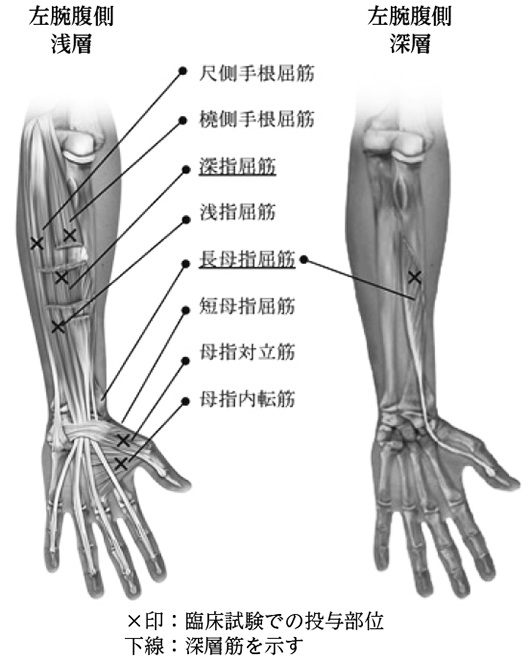
図 上肢痙縮関連筋 -
〈下肢痙縮〉
投与筋
投与部位数
(部位/筋)足関節の底屈(尖足)
腓腹筋(内側頭/外側頭)
50-200
2-6
ヒラメ筋
50-200
2-4
足関節の回外(内反)/底屈(尖足)
後脛骨筋
50-150
2-3
足趾の屈曲
長趾屈筋
50-100
1-3
長母趾屈筋
25-75
1-2
注11) 医師の判断により合計で最大400単位を配分注12) 投与部位一カ所につき最大1.0mLが推奨されている。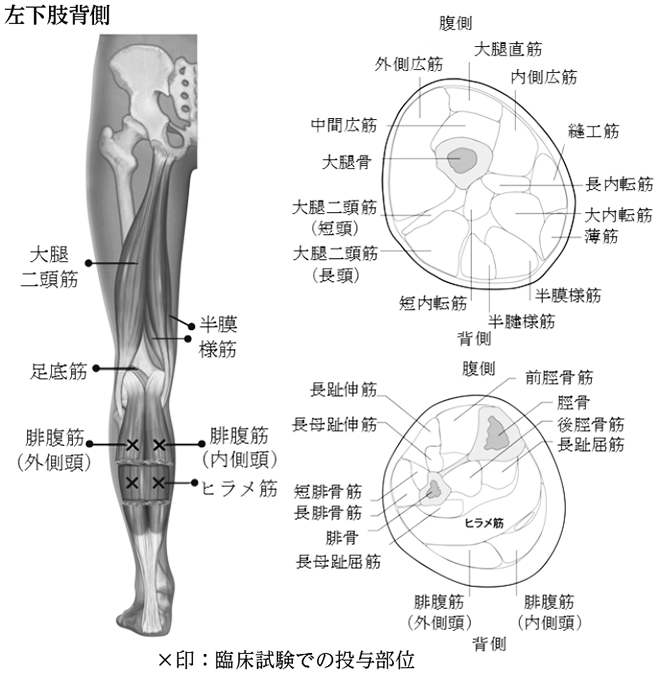
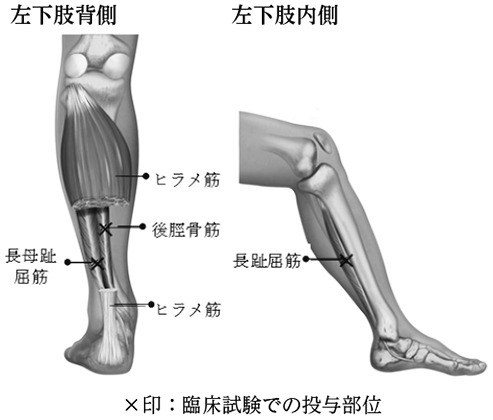
図 下肢痙縮関連筋
-
〈上肢痙縮〉
-
〈慢性流涎〉
- 7.7 *本剤と他のA型及びB型ボツリヌス毒素製剤の同時投与は避けること。本剤と他のA型及びB型ボツリヌス毒素製剤を同時投与した経験はない。[10.2 参照]
-
7.8 *投与に際して、解剖学的ランドマーク又は超音波検査を用いて注意深く唾液腺(耳下腺、顎下腺)を同定すること。臨床成績等から超音波検査での同定を推奨する。
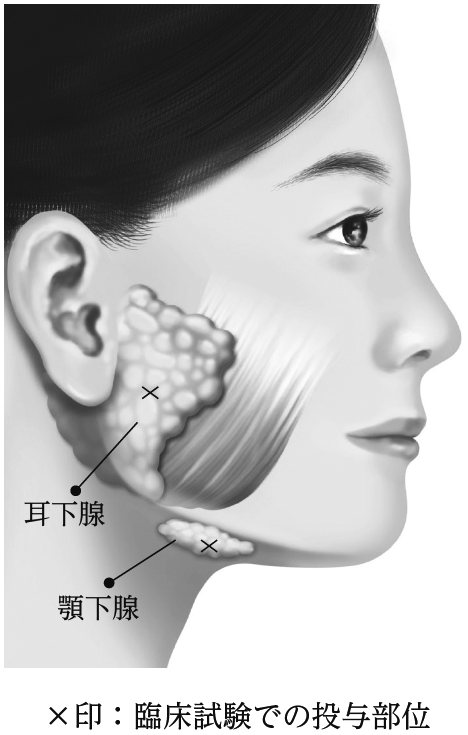
図 慢性流涎の投与対象唾液腺 - 7.9 *投与対象唾液腺ごとの適切な投与量に留意すること。臨床成績等から、以下の投与量及び投与部位数が推奨されている。[14.1.6 参照],[14.2.3 参照]
- 7.10 *患者の状態に応じて下表を参考に、本剤を減量することができる。[14.1.6 参照],[14.2.3 参照]
8. 重要な基本的注意
-
〈効能共通〉
-
8.1 本剤の投与に際しては、患者又はそれに代わる適切な者に、次の事項について文書を用いてよく説明し、文書による同意を得た後、使用すること。
- 本剤の有効成分は、ボツリヌス菌によって産生されるA型ボツリヌス毒素(一般的名称:インコボツリヌストキシンA)である。
- *本剤の投与は対症療法であり、その効果は上肢痙縮及び下肢痙縮では通常12-16週2) 、慢性流涎では通常16週3) ,4) で消失し、投与を繰り返す必要がある。
- 本剤投与により、投与部位以外の筋に対する影響と考えられる会話困難、嚥下障害及び誤嚥性肺炎等があらわれることがある。本剤投与開始から16週までに会話困難、嚥下障害及び呼吸困難等の体調の変化が生じた場合、直ちに医師の診察を受けること。
- 妊娠する可能性のある女性は、投与中及び最後の投与から16週後まで避妊を考慮すること。[9.4 参照],[9.5 参照]
- 他の医療施設でボツリヌス毒素の投与を受けている場合には、治療対象疾患及び投与日を必ず申し出ること。
- 8.2 本剤投与後、無力症、筋力低下があらわれることがあるので、自動車の運転等危険を伴う機械を操作する際には注意させること。
-
8.1 本剤の投与に際しては、患者又はそれに代わる適切な者に、次の事項について文書を用いてよく説明し、文書による同意を得た後、使用すること。
- 〈下肢痙縮〉
-
〈慢性流涎〉
- 8.4 *本剤の投与により口内乾燥があらわれることがあるため、患者又は介護者に対し本剤投与中は口腔内を清潔に保つように指導すること。
- 8.5 *慢性流涎患者では嚥下機能が低下していることから、本剤投与後は嚥下障害及び誤嚥性肺炎の発現に留意すること。本剤投与後にこれらの事象が発現した際には、本剤の効果が消失すると想定されるまでの期間は再投与を控えるとともに、再投与の可否は患者の状態を踏まえて慎重に検討すること。[11.1.2 参照]
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。 |
|
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。 |
|
慢性流涎患者においては、過剰な唾液分泌抑制があらわれるおそれがあり、口内乾燥、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに唾液分泌抑制作用を有するため作用が増強されるおそれがある。 |
|
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。 |
11. 副作用
11.1 重大な副作用
-
11.1.1 過敏症(頻度不明)
アナフィラキシーを含む重篤かつ即時型の過敏症、血清病等を起こす可能性があるので、呼吸困難、全身潮紅、血管浮腫、発疹、悪心等の症状が認められた場合には投与を中止し、血圧の維持、体液の補充管理、気道の確保等の適切な処置を行うこと。
-
11.1.2 嚥下障害
*嚥下障害(2.5%)、誤嚥性肺炎(0.2%)があらわれることがある。[8.5 参照]
11.2 その他の副作用
1~5%未満 |
1%未満 |
頻度不明 |
|
|---|---|---|---|
皮膚 |
湿疹、紅斑、蕁麻疹、過角化 |
そう痒症、発疹 |
|
*消化器 |
口内乾燥 |
便秘、口渇、唾液変性、味覚障害 |
悪心 |
筋骨格 |
筋力低下 |
四肢不快感、関節痛、筋骨格痛、筋肉痛、四肢痛、筋緊張低下 |
|
*精神神経系 |
麻痺、錯感覚、会話障害、頭痛、感覚鈍麻 |
血管迷走神経反応(一過性症候性低血圧、耳鳴、失神) |
|
*注射部位 |
皮下出血、注射部位内出血、筋肉内出血、疼痛 |
炎症、知覚異常、注射部位知覚低下、圧痛、注射部位腫脹、注射部位浮腫、紅斑、そう痒、感染、血腫、出血、挫傷 |
|
泌尿器 |
排尿後の尿滴下、頻尿、尿閉 |
||
*その他 |
構語障害、転倒、血中CK増加、靱帯捻挫、末梢性浮腫、倦怠感、蜂巣炎、無力症 |
軟部組織浮腫、腫脹、インフルエンザ様症状、上咽頭炎 |
14. 適用上の注意
14.1 薬剤調製時の注意
- 〈効能共通〉
-
〈上肢痙縮、下肢痙縮〉
-
14.1.5 本剤1バイアルは日局生理食塩液を用いて溶解する。
溶解液の量
(日局生理食塩液)溶解後のボツリヌス毒素濃度
50単位
0.25mL
20単位/0.1mL
0.5mL
10単位/0.1mL
1.0mL
5.0単位/0.1mL
1.25mL
4.0単位/0.1mL
2.0mL
2.5単位/0.1mL
2.5mL
2.0単位/0.1mL
4.0mL
1.25単位/0.1mL
5.0mL
1.0単位/0.1mL
溶解液の量
(日局生理食塩液)溶解後のボツリヌス毒素濃度
100単位
0.5mL
20単位/0.1mL
1.0mL
10単位/0.1mL
1.25mL
8.0単位/0.1mL
2.0mL
5.0単位/0.1mL
2.5mL
4.0単位/0.1mL
4.0mL
2.5単位/0.1mL
5.0mL
2.0単位/0.1mL
溶解液の量
(日局生理食塩液)溶解後のボツリヌス毒素濃度
200単位
0.5mL
40単位/0.1mL
1.0mL
20単位/0.1mL
1.25mL
16単位/0.1mL
2.0mL
10単位/0.1mL
2.5mL
8.0単位/0.1mL
4.0mL
5.0単位/0.1mL
5.0mL
4.0単位/0.1mL
-
14.1.5 本剤1バイアルは日局生理食塩液を用いて溶解する。
- 〈慢性流涎〉
14.2 薬剤投与時の注意
14.3 薬剤廃棄時の注意
残った薬液は、0.5%次亜塩素酸ナトリウム溶液を加える、又は滅菌処理(121℃、20分で高圧蒸気滅菌後に、120℃、10分で乾熱滅菌を行う)により失活させた後、密閉可能な廃棄袋又は箱に廃棄する。薬液の触れた器具等は同様に0.5%次亜塩素酸ナトリウム溶液をかける、又は滅菌処理(121℃、20分で高圧蒸気滅菌後に、120℃、10分で乾熱滅菌を行う)にかけて失活させた後、密閉可能な廃棄袋又は箱に廃棄する。
5. 効能又は効果に関連する注意
- 〈上肢痙縮、下肢痙縮〉
-
〈慢性流涎〉
- 5.4 *神経・筋疾患が原因となる慢性の流涎を有する患者に使用すること。
- 5.5 *臨床試験に組み入れられた患者の原疾患、重症度等の背景及び試験結果を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.3 参照],[17.1.4 参照]
- 5.6 *慢性流涎の原因となる疾患の診断及び治療を併せて行うこと。
6. 用法及び用量
-
〈上肢痙縮〉
通常、成人にはインコボツリヌストキシンAとして複数の緊張筋 注7) に合計400単位を分割して筋肉内注射する。1回あたりの最大投与量は400単位であるが、対象となる緊張筋の種類や数により、投与量は必要最小限となるよう適宜減量する。また、再投与は前回の効果が減弱した場合に可能であるが、投与間隔は12週以上とすること。なお、症状に応じて投与間隔は10週まで短縮できる。
注7) 緊張筋:橈側手根屈筋、尺側手根屈筋、浅指屈筋、深指屈筋、腕橈骨筋、上腕二頭筋、上腕筋、方形回内筋、円回内筋、長母指屈筋、母指内転筋、短母指屈筋/母指対立筋等 -
〈下肢痙縮〉
通常、成人にはインコボツリヌストキシンAとして複数の緊張筋 注8) に合計400単位を分割して筋肉内注射する。1回あたりの最大投与量は400単位であるが、対象となる緊張筋の種類や数により、投与量は必要最小限となるよう適宜減量する。また、再投与は前回の効果が減弱した場合に可能であるが、投与間隔は12週以上とすること。なお、症状に応じて投与間隔は10週まで短縮できる。
注8) 緊張筋:腓腹筋(内側頭、外側頭)、ヒラメ筋、後脛骨筋、長趾屈筋、長母趾屈筋等 -
〈慢性流涎〉
*通常、成人にはインコボツリヌストキシンAとして合計100単位を分割して両側の耳下腺(片側につき30単位)及び顎下腺(片側につき20単位)に注射するが、患者の状態により適宜減量する。また、再投与は前回の効果が減弱した場合に可能であるが、投与間隔は16週以上とすること。なお、患者の状態により投与間隔は14週まで短縮できる。
7. 用法及び用量に関連する注意
-
〈効能共通〉
-
7.1 *複数の適応に本剤を同時投与する場合には、それぞれの効能又は効果で規定されている投与量の上限及び投与間隔を厳守すること。
- 上肢痙縮及び下肢痙縮に対する同時投与では、合計で800単位を上限とし、患者の状態に応じて徐々に増量する等、慎重に投与すること。海外臨床試験において、上肢痙縮及び下肢痙縮に400単位から200単位ずつ増量し、合計800単位までを同時に投与した経験はあるが1) 、国内臨床試験では、上肢痙縮及び下肢痙縮に本剤を同時投与した経験はない。
- *上肢痙縮又は下肢痙縮と、慢性流涎に対して本剤を同時投与した経験はないため、同時投与は避けること。
- 7.2 本剤の力価(単位)は、A型ボツリヌス毒素製剤特有のもので、B型ボツリヌス毒素製剤とは異なること、また換算もできないことに留意し、必ず本剤の投与量を慎重に確認してから投与すること。
- 7.3 他のA型又はB型ボツリヌス毒素製剤を投与後に本剤を使用する場合には、少なくとも他のA型及びB型ボツリヌス毒素製剤の用法及び用量で規定されている投与間隔をあけるとともに、患者の症状を十分に観察した上で、効果が消失し、安全性上の問題がないと判断された場合にのみ投与すること。他のA型及びB型ボツリヌス毒素製剤の投与後12週以内に本剤を投与した場合の安全性及び有効性は確立していない。[10.2 参照]
-
7.1 *複数の適応に本剤を同時投与する場合には、それぞれの効能又は効果で規定されている投与量の上限及び投与間隔を厳守すること。
-
〈上肢痙縮、下肢痙縮〉
- 7.4 本剤と他のA型及びB型ボツリヌス毒素製剤の同時投与は原則として避けること。本剤と他のA型及びB型ボツリヌス毒素製剤を同時投与した際の、安全性及び有効性は確立していない。[10.2 参照]
- 7.5 緊張筋の同定が困難な場合には、筋電計、超音波検査やスティミュレーター等を用いて注意深く目標とする部位を同定すること。
-
7.6 筋ごとの適切な部位及び投与量に留意すること。臨床成績等から、以下のような投与筋、投与量及び投与部位数が推奨されている。[14.2.2 参照]
-
〈上肢痙縮〉
投与筋
投与部位数
(部位/筋)手関節の屈曲
橈側手根屈筋
25-100
1-2
尺側手根屈筋
20-100
1-2
手指関節の屈曲
浅指屈筋
25-100
1-2
深指屈筋
25-100
1-2
肘関節の屈曲
腕橈骨筋
25-100
1-3
上腕二頭筋
50-200
2-4
上腕筋
25-100
1-2
前腕の回内
方形回内筋
10-50
1
円回内筋
25-75
1-2
母指関節の屈曲
長母指屈筋
10-50
1
母指内転筋
5-30
1
短母指屈筋又は母指対立筋
5-30
1
注9) 医師の判断により合計で最大400単位を配分注10) 投与部位一カ所につき最大1.0mLが推奨されている。

図 上肢痙縮関連筋 -
〈下肢痙縮〉
投与筋
投与部位数
(部位/筋)足関節の底屈(尖足)
腓腹筋(内側頭/外側頭)
50-200
2-6
ヒラメ筋
50-200
2-4
足関節の回外(内反)/底屈(尖足)
後脛骨筋
50-150
2-3
足趾の屈曲
長趾屈筋
50-100
1-3
長母趾屈筋
25-75
1-2
注11) 医師の判断により合計で最大400単位を配分注12) 投与部位一カ所につき最大1.0mLが推奨されている。

図 下肢痙縮関連筋
-
〈上肢痙縮〉
-
〈慢性流涎〉
- 7.7 *本剤と他のA型及びB型ボツリヌス毒素製剤の同時投与は避けること。本剤と他のA型及びB型ボツリヌス毒素製剤を同時投与した経験はない。[10.2 参照]
-
7.8 *投与に際して、解剖学的ランドマーク又は超音波検査を用いて注意深く唾液腺(耳下腺、顎下腺)を同定すること。臨床成績等から超音波検査での同定を推奨する。

図 慢性流涎の投与対象唾液腺 - 7.9 *投与対象唾液腺ごとの適切な投与量に留意すること。臨床成績等から、以下の投与量及び投与部位数が推奨されている。[14.1.6 参照],[14.2.3 参照]
- 7.10 *患者の状態に応じて下表を参考に、本剤を減量することができる。[14.1.6 参照],[14.2.3 参照]
8. 重要な基本的注意
-
〈効能共通〉
-
8.1 本剤の投与に際しては、患者又はそれに代わる適切な者に、次の事項について文書を用いてよく説明し、文書による同意を得た後、使用すること。
- 本剤の有効成分は、ボツリヌス菌によって産生されるA型ボツリヌス毒素(一般的名称:インコボツリヌストキシンA)である。
- *本剤の投与は対症療法であり、その効果は上肢痙縮及び下肢痙縮では通常12-16週2) 、慢性流涎では通常16週3) ,4) で消失し、投与を繰り返す必要がある。
- 本剤投与により、投与部位以外の筋に対する影響と考えられる会話困難、嚥下障害及び誤嚥性肺炎等があらわれることがある。本剤投与開始から16週までに会話困難、嚥下障害及び呼吸困難等の体調の変化が生じた場合、直ちに医師の診察を受けること。
- 妊娠する可能性のある女性は、投与中及び最後の投与から16週後まで避妊を考慮すること。[9.4 参照],[9.5 参照]
- 他の医療施設でボツリヌス毒素の投与を受けている場合には、治療対象疾患及び投与日を必ず申し出ること。
- 8.2 本剤投与後、無力症、筋力低下があらわれることがあるので、自動車の運転等危険を伴う機械を操作する際には注意させること。
-
8.1 本剤の投与に際しては、患者又はそれに代わる適切な者に、次の事項について文書を用いてよく説明し、文書による同意を得た後、使用すること。
- 〈下肢痙縮〉
-
〈慢性流涎〉
- 8.4 *本剤の投与により口内乾燥があらわれることがあるため、患者又は介護者に対し本剤投与中は口腔内を清潔に保つように指導すること。
- 8.5 *慢性流涎患者では嚥下機能が低下していることから、本剤投与後は嚥下障害及び誤嚥性肺炎の発現に留意すること。本剤投与後にこれらの事象が発現した際には、本剤の効果が消失すると想定されるまでの期間は再投与を控えるとともに、再投与の可否は患者の状態を踏まえて慎重に検討すること。[11.1.2 参照]
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。 |
|
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。 |
|
慢性流涎患者においては、過剰な唾液分泌抑制があらわれるおそれがあり、口内乾燥、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに唾液分泌抑制作用を有するため作用が増強されるおそれがある。 |
|
過剰な筋弛緩があらわれるおそれがあり、筋力低下、嚥下障害等の発現するリスクが高まるおそれがある。 |
本剤及びこれらの薬剤はともに筋弛緩作用を有するため作用が増強されるおそれがある。 |
11. 副作用
11.1 重大な副作用
-
11.1.1 過敏症(頻度不明)
アナフィラキシーを含む重篤かつ即時型の過敏症、血清病等を起こす可能性があるので、呼吸困難、全身潮紅、血管浮腫、発疹、悪心等の症状が認められた場合には投与を中止し、血圧の維持、体液の補充管理、気道の確保等の適切な処置を行うこと。
-
11.1.2 嚥下障害
*嚥下障害(2.5%)、誤嚥性肺炎(0.2%)があらわれることがある。[8.5 参照]
11.2 その他の副作用
1~5%未満 |
1%未満 |
頻度不明 |
|
|---|---|---|---|
皮膚 |
湿疹、紅斑、蕁麻疹、過角化 |
そう痒症、発疹 |
|
*消化器 |
口内乾燥 |
便秘、口渇、唾液変性、味覚障害 |
悪心 |
筋骨格 |
筋力低下 |
四肢不快感、関節痛、筋骨格痛、筋肉痛、四肢痛、筋緊張低下 |
|
*精神神経系 |
麻痺、錯感覚、会話障害、頭痛、感覚鈍麻 |
血管迷走神経反応(一過性症候性低血圧、耳鳴、失神) |
|
*注射部位 |
皮下出血、注射部位内出血、筋肉内出血、疼痛 |
炎症、知覚異常、注射部位知覚低下、圧痛、注射部位腫脹、注射部位浮腫、紅斑、そう痒、感染、血腫、出血、挫傷 |
|
泌尿器 |
排尿後の尿滴下、頻尿、尿閉 |
||
*その他 |
構語障害、転倒、血中CK増加、靱帯捻挫、末梢性浮腫、倦怠感、蜂巣炎、無力症 |
軟部組織浮腫、腫脹、インフルエンザ様症状、上咽頭炎 |
14. 適用上の注意
14.1 薬剤調製時の注意
- 〈効能共通〉
-
〈上肢痙縮、下肢痙縮〉
-
14.1.5 本剤1バイアルは日局生理食塩液を用いて溶解する。
溶解液の量
(日局生理食塩液)溶解後のボツリヌス毒素濃度
50単位
0.25mL
20単位/0.1mL
0.5mL
10単位/0.1mL
1.0mL
5.0単位/0.1mL
1.25mL
4.0単位/0.1mL
2.0mL
2.5単位/0.1mL
2.5mL
2.0単位/0.1mL
4.0mL
1.25単位/0.1mL
5.0mL
1.0単位/0.1mL
溶解液の量
(日局生理食塩液)溶解後のボツリヌス毒素濃度
100単位
0.5mL
20単位/0.1mL
1.0mL
10単位/0.1mL
1.25mL
8.0単位/0.1mL
2.0mL
5.0単位/0.1mL
2.5mL
4.0単位/0.1mL
4.0mL
2.5単位/0.1mL
5.0mL
2.0単位/0.1mL
溶解液の量
(日局生理食塩液)溶解後のボツリヌス毒素濃度
200単位
0.5mL
40単位/0.1mL
1.0mL
20単位/0.1mL
1.25mL
16単位/0.1mL
2.0mL
10単位/0.1mL
2.5mL
8.0単位/0.1mL
4.0mL
5.0単位/0.1mL
5.0mL
4.0単位/0.1mL
-
14.1.5 本剤1バイアルは日局生理食塩液を用いて溶解する。
- 〈慢性流涎〉
14.2 薬剤投与時の注意
14.3 薬剤廃棄時の注意
残った薬液は、0.5%次亜塩素酸ナトリウム溶液を加える、又は滅菌処理(121℃、20分で高圧蒸気滅菌後に、120℃、10分で乾熱滅菌を行う)により失活させた後、密閉可能な廃棄袋又は箱に廃棄する。薬液の触れた器具等は同様に0.5%次亜塩素酸ナトリウム溶液をかける、又は滅菌処理(121℃、20分で高圧蒸気滅菌後に、120℃、10分で乾熱滅菌を行う)にかけて失活させた後、密閉可能な廃棄袋又は箱に廃棄する。