薬効分類名経皮吸収型ドパミン作動性パーキンソン病治療剤
一般的名称ロピニロール塩酸塩経皮吸収型製剤
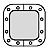
ハルロピテープ8mg、ハルロピテープ16mg、ハルロピテープ24mg、ハルロピテープ32mg、ハルロピテープ40mg
はるろぴてーぷ、はるろぴてーぷ、はるろぴてーぷ、はるろぴてーぷ、はるろぴてーぷ
HARUROPI Tapes, HARUROPI Tapes, HARUROPI Tapes, HARUROPI Tapes, HARUROPI Tapes
製造販売元/久光製薬株式会社、発売元/協和キリン株式会社
重大な副作用
その他の副作用
併用注意
- ドパミン拮抗剤
本剤の作用が減弱することがある。
本剤はドパミン受容体作動薬であり、併用により両薬剤の作用が拮抗するおそれがある。
- CYP1A2阻害作用を有する薬剤
ロピニロール速放錠とシプロフロキサシンとの併用によりロピニロールのCmax及びAUCがそれぞれ約60%及び84%増加したことが報告されている。本剤使用中にこれらの薬剤を投与開始又は中止する場合は、必要に応じて本剤の用量を調整すること。
これらの薬剤のCYP1A2阻害作用により、本剤の血中濃度が上昇する可能性がある。
- エストロゲン含有製剤
高用量のエストロゲンを投与した患者でロピニロールの血中濃度上昇がみられたとの報告があるので、本剤使用中に高用量のエストロゲンを投与開始又は中止する場合は、必要に応じて本剤の用量を調整すること。
機序不明
1. 警告
前兆のない突発的睡眠及び傾眠等がみられることがあり、またドパミン受容体作動薬の投与において、突発的睡眠により自動車事故を起こした例が報告されているので、患者に本剤の突発的睡眠及び傾眠等についてよく説明し、本剤使用中には、自動車の運転、機械の操作、高所作業等危険を伴う作業に従事させないよう注意すること。[8.1 参照],[11.1.1 参照]
2. 禁忌(次の患者には投与しないこと)
- 2.1 本剤の成分に対し過敏症の既往歴のある患者
- 2.2 妊婦又は妊娠している可能性のある女性[9.5 参照]
4. 効能又は効果
パーキンソン病
6. 用法及び用量
通常、成人にはロピニロール塩酸塩として1日1回8mgから始め、以後経過を観察しながら、必要に応じて1週間以上の間隔で、1日量として8mgずつ増量する。いずれの投与量の場合も1日1回、胸部、腹部、側腹部、大腿部又は上腕部のいずれかの皮膚に貼付し、24時間毎に貼り替える。なお、年齢、症状により適宜増減するが、ロピニロール塩酸塩として1日量64mgを超えないこととする。
7. 用法及び用量に関連する注意
使用は「6.用法及び用量」に従い少量から始め、消化器症状(悪心、嘔吐等)、血圧等の観察を十分に行いながら慎重に増量し、患者毎に適切な維持量を定めること。
8. 重要な基本的注意
- 8.1 ドパミン受容体作動薬の投与において、突発的睡眠により自動車事故を起こした例が報告されている。患者には突発的睡眠及び傾眠等についてよく説明し、自動車の運転、機械の操作、高所作業等危険を伴う作業に従事させないよう注意すること。なお、海外において突発的睡眠を起こした症例の中には、傾眠や過度の眠気のような前兆を認めなかった例あるいは投与開始後1年以上経過した後に初めて発現した例も報告されている。[1 参照],[11.1.1 参照]
- 8.2 起立性低血圧がみられることがあるので、使用は少量から始め、めまい、立ちくらみ、ふらつき等の起立性低血圧の徴候や症状が認められた場合には、減量、休薬又は使用中止等の適切な処置を行うこと。
- 8.3 減量、中止が必要な場合は、漸減すること。急激な減量又は中止により、高熱、意識障害、高度の筋硬直、不随意運動、ショック症状等の悪性症候群があらわれることがある。また、ドパミン受容体作動薬の急激な減量又は中止により、薬剤離脱症候群(無感情、不安、うつ、疲労感、発汗、疼痛等の症状を特徴とする)があらわれることがある。[11.1.3 参照]
- 8.4 レボドパ又はドパミン受容体作動薬の投与により、病的賭博(個人的生活の崩壊等の社会的に不利な結果を招くにもかかわらず、持続的にギャンブルを繰り返す状態)、病的性欲亢進、強迫性購買、暴食等の衝動制御障害が報告されているので、このような症状が発現した場合には、減量又は使用を中止するなど適切な処置を行うこと。また、患者及び家族等にこのような衝動制御障害の症状について説明すること。
- 8.5 貼付により皮膚症状を起こすことがあるので、貼付箇所を毎回変更すること。皮膚症状があらわれた場合には、ステロイド軟膏等を投与する、本剤を使用中止するなど適切な処置を行うこと。
- 8.6 貼付してある製剤を除去せずに新たな製剤を貼付した場合、血中濃度が上昇するため、貼り替えの際は先に貼付した製剤を除去したことを十分に確認するよう患者及び介護者等に指導すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 幻覚、妄想等の精神症状又はそれらの既往のある患者
症状が増悪又は発現しやすくなることがある。[11.1.2 参照]
-
9.1.2 重篤な心疾患又はその既往歴のある患者
薬理作用から心拍数低下を起こす可能性がある。
-
9.1.3 低血圧症の患者
症状が悪化することがある。
9.2 腎機能障害患者
9.3 肝機能障害患者
主として肝臓で代謝される。また、これらの患者を対象とした臨床試験は実施していない。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には使用しないこと。動物実験(ラット)で胎児毒性(体重減少、死亡数増加及び指の奇形)が報告されている。[2.2 参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒトにおいて血漿中プロラクチン濃度の低下が認められることが報告されており、乳汁分泌が抑制されるおそれがある。また、動物実験(ラット)で乳汁中に移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下している。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
本剤の作用が減弱することがある。 |
本剤はドパミン受容体作動薬であり、併用により両薬剤の作用が拮抗するおそれがある。 |
|
ロピニロール速放錠とシプロフロキサシンとの併用によりロピニロールのCmax及びAUCがそれぞれ約60%及び84%増加したことが報告されている。本剤使用中にこれらの薬剤を投与開始又は中止する場合は、必要に応じて本剤の用量を調整すること。 |
これらの薬剤のCYP1A2阻害作用により、本剤の血中濃度が上昇する可能性がある。 |
|
高用量のエストロゲンを投与した患者でロピニロールの血中濃度上昇がみられたとの報告があるので、本剤使用中に高用量のエストロゲンを投与開始又は中止する場合は、必要に応じて本剤の用量を調整すること。 |
機序不明 |
|
|
ジスキネジア、幻覚、錯乱等の副作用が増強することがある。 |
相互に作用が増強することがある。 |
11. 副作用
11.1 重大な副作用
- 11.1.1 突発的睡眠(0.7%)、極度の傾眠(頻度不明)
-
11.1.2 幻覚(3.6%)、妄想(0.4%)、興奮(0.1%)、錯乱(頻度不明)、譫妄(0.7%)
幻覚、妄想、興奮、錯乱、譫妄等の精神症状があらわれることがある。[9.1.1 参照],[10.2 参照]
-
11.1.3 悪性症候群(頻度不明)
使用後、減量後又は中止後に、高熱、意識障害、高度の筋硬直、不随意運動、ショック症状等があらわれることがある。このような症状があらわれた場合には、使用開始初期の場合は中止し、また、継続使用中の用量変更・中止時の場合は一旦もとの使用量に戻した後、慎重に漸減し、体冷却、水分補給等の適切な処置を行うこと。なお、使用継続中にも同様の症状があらわれることがある。[8.3 参照]
11.2 その他の副作用
5%以上 |
1%以上5%未満 |
1%未満 |
頻度不明 |
|
|---|---|---|---|---|
精神神経系 |
傾眠、ジスキネジア |
幻視、浮動性めまい、体位性めまい、頭痛、不眠 |
錯覚、ジストニア、幻聴、リビドー亢進、回転性めまい |
衝動制御障害(病的賭博、病的性欲亢進、強迫性購買、暴食等)、躁状態 |
肝臓 |
ALT上昇、AST上昇、γ-GTP上昇 |
肝機能異常、ビリルビン上昇、AL-P上昇 |
||
筋・骨格系 |
姿勢異常、CK上昇 |
背部痛 |
||
循環器 |
起立性低血圧、起立血圧低下 |
上室性期外収縮、心室性期外収縮、動悸、低血圧、血圧上昇 |
||
消化器 |
悪心、便秘 |
食欲不振、嘔吐、腹部不快感 |
下痢、消化不良 |
|
腎臓 |
尿潜血陽性 |
BUN上昇、尿蛋白陽性 |
||
皮膚 |
適用部位紅斑、適用部位そう痒感 |
適用部位皮膚炎、適用部位発疹、適用部位刺激感、適用部位腫脹、適用部位色素沈着 |
||
過敏症 |
発疹、湿疹、そう痒、顔面浮腫、じん麻疹 |
|||
その他 |
けん怠感、末梢性浮腫、LDH上昇 |
異常感、転倒、胸部不快感、浮腫、口渇、挫傷、咳嗽、好酸球増加、尿糖陽性 |
薬剤離脱症候群 注1) (無感情、不安、うつ、疲労感、発汗、疼痛等) |
1. 警告
前兆のない突発的睡眠及び傾眠等がみられることがあり、またドパミン受容体作動薬の投与において、突発的睡眠により自動車事故を起こした例が報告されているので、患者に本剤の突発的睡眠及び傾眠等についてよく説明し、本剤使用中には、自動車の運転、機械の操作、高所作業等危険を伴う作業に従事させないよう注意すること。[8.1 参照],[11.1.1 参照]
2. 禁忌(次の患者には投与しないこと)
- 2.1 本剤の成分に対し過敏症の既往歴のある患者
- 2.2 妊婦又は妊娠している可能性のある女性[9.5 参照]
4. 効能又は効果
パーキンソン病
6. 用法及び用量
通常、成人にはロピニロール塩酸塩として1日1回8mgから始め、以後経過を観察しながら、必要に応じて1週間以上の間隔で、1日量として8mgずつ増量する。いずれの投与量の場合も1日1回、胸部、腹部、側腹部、大腿部又は上腕部のいずれかの皮膚に貼付し、24時間毎に貼り替える。なお、年齢、症状により適宜増減するが、ロピニロール塩酸塩として1日量64mgを超えないこととする。
7. 用法及び用量に関連する注意
使用は「6.用法及び用量」に従い少量から始め、消化器症状(悪心、嘔吐等)、血圧等の観察を十分に行いながら慎重に増量し、患者毎に適切な維持量を定めること。
8. 重要な基本的注意
- 8.1 ドパミン受容体作動薬の投与において、突発的睡眠により自動車事故を起こした例が報告されている。患者には突発的睡眠及び傾眠等についてよく説明し、自動車の運転、機械の操作、高所作業等危険を伴う作業に従事させないよう注意すること。なお、海外において突発的睡眠を起こした症例の中には、傾眠や過度の眠気のような前兆を認めなかった例あるいは投与開始後1年以上経過した後に初めて発現した例も報告されている。[1 参照],[11.1.1 参照]
- 8.2 起立性低血圧がみられることがあるので、使用は少量から始め、めまい、立ちくらみ、ふらつき等の起立性低血圧の徴候や症状が認められた場合には、減量、休薬又は使用中止等の適切な処置を行うこと。
- 8.3 減量、中止が必要な場合は、漸減すること。急激な減量又は中止により、高熱、意識障害、高度の筋硬直、不随意運動、ショック症状等の悪性症候群があらわれることがある。また、ドパミン受容体作動薬の急激な減量又は中止により、薬剤離脱症候群(無感情、不安、うつ、疲労感、発汗、疼痛等の症状を特徴とする)があらわれることがある。[11.1.3 参照]
- 8.4 レボドパ又はドパミン受容体作動薬の投与により、病的賭博(個人的生活の崩壊等の社会的に不利な結果を招くにもかかわらず、持続的にギャンブルを繰り返す状態)、病的性欲亢進、強迫性購買、暴食等の衝動制御障害が報告されているので、このような症状が発現した場合には、減量又は使用を中止するなど適切な処置を行うこと。また、患者及び家族等にこのような衝動制御障害の症状について説明すること。
- 8.5 貼付により皮膚症状を起こすことがあるので、貼付箇所を毎回変更すること。皮膚症状があらわれた場合には、ステロイド軟膏等を投与する、本剤を使用中止するなど適切な処置を行うこと。
- 8.6 貼付してある製剤を除去せずに新たな製剤を貼付した場合、血中濃度が上昇するため、貼り替えの際は先に貼付した製剤を除去したことを十分に確認するよう患者及び介護者等に指導すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
-
9.1.1 幻覚、妄想等の精神症状又はそれらの既往のある患者
症状が増悪又は発現しやすくなることがある。[11.1.2 参照]
-
9.1.2 重篤な心疾患又はその既往歴のある患者
薬理作用から心拍数低下を起こす可能性がある。
-
9.1.3 低血圧症の患者
症状が悪化することがある。
9.2 腎機能障害患者
9.3 肝機能障害患者
主として肝臓で代謝される。また、これらの患者を対象とした臨床試験は実施していない。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には使用しないこと。動物実験(ラット)で胎児毒性(体重減少、死亡数増加及び指の奇形)が報告されている。[2.2 参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒトにおいて血漿中プロラクチン濃度の低下が認められることが報告されており、乳汁分泌が抑制されるおそれがある。また、動物実験(ラット)で乳汁中に移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下している。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
本剤の作用が減弱することがある。 |
本剤はドパミン受容体作動薬であり、併用により両薬剤の作用が拮抗するおそれがある。 |
|
ロピニロール速放錠とシプロフロキサシンとの併用によりロピニロールのCmax及びAUCがそれぞれ約60%及び84%増加したことが報告されている。本剤使用中にこれらの薬剤を投与開始又は中止する場合は、必要に応じて本剤の用量を調整すること。 |
これらの薬剤のCYP1A2阻害作用により、本剤の血中濃度が上昇する可能性がある。 |
|
高用量のエストロゲンを投与した患者でロピニロールの血中濃度上昇がみられたとの報告があるので、本剤使用中に高用量のエストロゲンを投与開始又は中止する場合は、必要に応じて本剤の用量を調整すること。 |
機序不明 |
|
|
ジスキネジア、幻覚、錯乱等の副作用が増強することがある。 |
相互に作用が増強することがある。 |
11. 副作用
11.1 重大な副作用
- 11.1.1 突発的睡眠(0.7%)、極度の傾眠(頻度不明)
-
11.1.2 幻覚(3.6%)、妄想(0.4%)、興奮(0.1%)、錯乱(頻度不明)、譫妄(0.7%)
幻覚、妄想、興奮、錯乱、譫妄等の精神症状があらわれることがある。[9.1.1 参照],[10.2 参照]
-
11.1.3 悪性症候群(頻度不明)
使用後、減量後又は中止後に、高熱、意識障害、高度の筋硬直、不随意運動、ショック症状等があらわれることがある。このような症状があらわれた場合には、使用開始初期の場合は中止し、また、継続使用中の用量変更・中止時の場合は一旦もとの使用量に戻した後、慎重に漸減し、体冷却、水分補給等の適切な処置を行うこと。なお、使用継続中にも同様の症状があらわれることがある。[8.3 参照]
11.2 その他の副作用
5%以上 |
1%以上5%未満 |
1%未満 |
頻度不明 |
|
|---|---|---|---|---|
精神神経系 |
傾眠、ジスキネジア |
幻視、浮動性めまい、体位性めまい、頭痛、不眠 |
錯覚、ジストニア、幻聴、リビドー亢進、回転性めまい |
衝動制御障害(病的賭博、病的性欲亢進、強迫性購買、暴食等)、躁状態 |
肝臓 |
ALT上昇、AST上昇、γ-GTP上昇 |
肝機能異常、ビリルビン上昇、AL-P上昇 |
||
筋・骨格系 |
姿勢異常、CK上昇 |
背部痛 |
||
循環器 |
起立性低血圧、起立血圧低下 |
上室性期外収縮、心室性期外収縮、動悸、低血圧、血圧上昇 |
||
消化器 |
悪心、便秘 |
食欲不振、嘔吐、腹部不快感 |
下痢、消化不良 |
|
腎臓 |
尿潜血陽性 |
BUN上昇、尿蛋白陽性 |
||
皮膚 |
適用部位紅斑、適用部位そう痒感 |
適用部位皮膚炎、適用部位発疹、適用部位刺激感、適用部位腫脹、適用部位色素沈着 |
||
過敏症 |
発疹、湿疹、そう痒、顔面浮腫、じん麻疹 |
|||
その他 |
けん怠感、末梢性浮腫、LDH上昇 |
異常感、転倒、胸部不快感、浮腫、口渇、挫傷、咳嗽、好酸球増加、尿糖陽性 |
薬剤離脱症候群 注1) (無感情、不安、うつ、疲労感、発汗、疼痛等) |